Архе́и - архебактерии, группа микроскопических одноклеточных организмов; относятся к «доядерным» формам - прокариотам. Сходны с истинными бактериями по размерам клеток и морфологическим признакам, однако состав и строение клеточных стенок, структура генетического аппарата и другие особенности сближают их с эукариотами. Описано более 100 видов. Большинство археев живёт в экстремальных условиях, часто непригодных для жизни других организмов, - в насыщенных растворах солей (галобактерии), при температуре 80ºC и выше (гипертермофилы), в кислой среде (pH 1-2, термоплазмы) и т. д. Только среди археев есть метаногены - организмы, способные выделять газ метан. Археи, как и бактерии, относятся к наиболее древним обитателям Земли.
хлор
Энциклопедический словарь
ХЛОР -а; м. [от греч. chlōros - бледно-зелёный] Химический элемент (Cl), удушливый газ зеленовато-жёлтого цвета с резким запахом (используется как отравляющее и обеззараживающее средство). Соединения хлора. Отравление хлором.
◁ Хло́рный (см.).
* * *
хлор (лат. Chlorum), химический элемент VII группы периодической системы, относится к галогенам. Название от греческого chlōros - жёлто-зелёный. Свободный хлор состоит из двухатомных молекул (Cl2); газ жёлто-зелёного цвета с резким запахом; плотность 3,214 г/л; tпл -101°C; tкип -33,97°C; при обычной температуре легко сжижается под давлением 0,6 МПа. Химически очень активен (окислитель). Главные минералы - галит (каменная соль), сильвин, бишофит; морская вода содержит хлориды натрия, калия, магния и других элементов. Применяют в производстве хлорсодержащих органических соединений (60-75%), неорганических веществ (10-20%), для отбеливания целлюлозы и тканей (5-15%), для санитарных нужд и обеззараживания (хлорирования) воды. Токсичен.
* * *
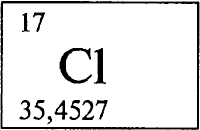
ХЛОР - ХЛОР (лат. Сhlorum), Cl (читается «хлор»), химический элемент с атомным номером 17, атомная масса 35,453. В свободном виде - желто-зеленый тяжелый газ с резким удушливым запахом (отсюда название: греч. chloros - желто-зеленый).
Природный хлор представляет смесь двух нуклидов (см. НУКЛИД) с массовыми числами 35 (в смеси 75,77% по массе) и 37 (24,23%). Конфигурация внешнего электронного слоя 3s2p5. В соединениях проявляет главным образом степени окисления -1, +1, +3, +5 и +7 (валентности I, III, V и VII). Расположен в третьем периоде в группе VIIА периодической системы элементов Менделеева, относится к галогенам (см. ГАЛОГЕНЫ).
Радиус нейтрального атома хлора 0,099 нм, ионные радиусы равны, соответственно (в скобках указаны значения координационного числа): Cl- 0,167 нм (6), Cl5+ 0,026 нм (3) и Clr7+ 0,022 нм (3) и 0,041 нм (6). Энергии последовательной ионизации нейтрального атома хлора равны, соответственно, 12,97, 23,80, 35,9, 53,5, 67,8, 96,7 и 114,3 эВ. Сродство к электрону 3,614 эВ. По шкале Полинга электроотрицательность хлора 3,16.
История открытия
Важнейшее химическое соединение хлора - поваренная соль (химическая формула NaCl, химическое название хлорид натрия) - было известно человеку с древнейших времен. Имеются свидетельства того, что добыча поваренной соли осуществлялась еще 3-4 тысячи лет до нашей эры в Ливии. Возможно, что, используя поваренную соль для различных манипуляций, алхимики сталкивались и с газообразным хлором. Для растворения «царя металлов» - золота - они использовали «царскую водку» - смесь соляной и азотной кислот, при взаимодействии которых выделяется хлор.
Впервые газ хлор получил и подробно описал шведский химик К. Шееле (см. ШЕЕЛЕ Карл Вильгельм) в 1774 году. Он нагревал соляную кислоту с минералом пиролюзитом (см. ПИРОЛЮЗИТ) MnO2 и наблюдал выделение желто-зеленого газа с резким запахом. Так как в те времена господствовала теория флогистона (см. ФЛОГИСТОН), новый газ Шееле рассматривал как «дефлогистонированную соляную кислоту», т. е. как окись (оксид) соляной кислоты. А.Лавуазье (см. ЛАВУАЗЬЕ Антуан Лоран) рассматривал газ как оксид элемента «мурия» (соляную кислоту называли муриевой, от лат. muria - рассол). Такую же точку зрения сначала разделял английский ученый Г. Дэви (см. ДЭВИ Гемфри), который потратил много времени на то, чтобы разложить «окись мурия» на простые вещества. Это ему не удалось, и к 1811 году Дэви пришел к выводу, что данный газ - это простое вещество, и ему отвечает химический элемент. Дэви первым предложил в соответствие с желто-зеленой окраской газа назвать его chlorine (хлорин). Название «хлор» элементу дал в 1812 французский химик Ж. Л. Гей-Люссак (см. ГЕЙ-ЛЮССАК Жозеф Луи); оно принято во всех странах, кроме Великобритании и США, где сохранилось название, введенное Дэви. Высказывалось мнение о том, что данный элемент следует назвать «галоген» (т. е. рождающий соли), но оно со временем стало общим названием всех элементов группы VIIA.
Нахождение в природе
Содержание хлора в земной коре составляет 0,013% по массе, в заметной концентрации он в виде иона Cl- присутствует в морской воде (в среднем около 18,8 г/л). Химически хлор высоко активен и поэтому в свободном виде в природе не встречается. Он входит в состав таких минералов, образующих большие залежи, как поваренная, или каменная, соль (галит (см. ГАЛИТ)) NaCl, карналлит (см. КАРНАЛЛИТ) KCl·MgCl2·6H21O, сильвин (см. СИЛЬВИН) КСl, сильвинит (Na, K)Cl, каинит (см. КАИНИТ) КСl·MgSO4·3Н2О, бишофит (см. БИШОФИТ) MgCl2·6H2O и многих других. Хлор можно обнаружить в самых разных породах, в почве.
Получение
Для получения газообразного хлора используют электролиз крепкого водного раствора NaCl (иногда используют KCl). Электролиз проводят с использованием катионообменной мембраны, разделяющей катодное и анодное пространства. При этом за счет процесса
2NaCl + 2H2O = 2NaOH + H2 + Cl2
получают сразу три ценных химических продукта: на аноде - хлор, на катоде - водород (см. ВОДОРОД) , и в электролизере накапливается щелочь (1,13 тонны NaOH на каждую тонну полученного хлора). Производство хлора электролизом требует больших затрат электроэнергии: на получение1 т хлора расходуется от 2,3 до 3,7 МВт.
Для получения хлора в лаборатории используют реакцию концентрированной соляной кислоты с каким-либо сильным окислителем (перманганатом калия KMnO4, дихроматом калия K2Cr2O7, хлоратом калия KClO3, хлорной известью CaClOCl, оксидом марганца (IV) MnO2). Наиболее удобно использовать для этих целей перманганат калия: в этом случае реакция протекает без нагревания:
2KMnO4 + 16HCl = 2KСl + 2MnCl2+ 5Cl2+ 8H2O.
При необходимости хлор в сжиженном (под давлением) виде транспортируют в железнодорожных цистернах или в стальных баллонах. Баллоны с хлором имеют специальную маркировку, но даже при ее отсутствии хлорный баллон легко отличить от баллонов с другими неядовитыми газами. Дно хлорных баллонов имеет форму полушария, и баллон с жидким хлором невозможно без опоры поставить вертикально.
Физические и химические свойства
При обычных условиях хлор - желто-зеленый газ, плотность газа при 25°C 3,214 г/дм3 (примерно в 2,5 раза больше плотности воздуха). Температура плавления твердого хлора -100,98°C, температура кипения -33,97°C. Стандартный электродный потенциал Сl2/Сl- в водном растворе равен +1,3583 В.
В свободном состоянии существует в виде двухатомных молекул Сl2. Межъядерное расстояние в этой молекуле 0,1987 нм. Сродство к электрону молекулы Сl2 2,45 эВ, потенциал ионизации 11,48 эВ. Энергия диссоциации молекул Сl2 на атомы сравнительно невелика и составляет 239,23 кДж/моль.
Хлор немного растворим в воде. При температуре 0°C растворимость составляет 1,44 масс.%, при 20°C - 0,711°C масс.%, при 60°C - 0,323 масс. %. Раствор хлора в воде называют хлорной водой. В хлорной воде устанавливается равновесие:
Сl2 + H2O H+ = Сl- + HOСl.
Для того, чтобы сместить это равновесие влево, т. е. понизить растворимость хлора в воде, в воду следует добавить или хлорид натрия NaCl, или какую-либо нелетучую сильную кислоту (например, серную).
Хлор хорошо растворим во многих неполярных жидкостях. Жидкий хлор сам служит растворителем таких веществ, как ВСl3, SiCl4, TiCl4.
Из-за низкой энергии диссоциации молекул Сl2 на атомы и высокого сродства атома хлора к электрону химически хлор высоко активен. Он вступает в непосредственное взаимодействие с большинством металлов (в том числе, например, с золотом) и многими неметаллами. Так, без нагревания хлор реагирует с щелочными (см. ЩЕЛОЧНЫЕ МЕТАЛЛЫ) и щелочноземельными металлами (см. ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ), с сурьмой:
2Sb + 3Cl2 = 2SbCl3
При нагревании хлор реагирует с алюминием:
3Сl2 + 2Аl = 2А1Сl3
и железом:
2Fe + 3Cl2 = 2FeCl3.
С водородом H2 хлор реагирует или при поджигании (хлор спокойно горит в атмосфере водорода), или при облучении смеси хлора и водорода ультрафиолетовым светом. При этом возникает газ хлороводород НСl:
Н2 + Сl2 = 2НСl.
Раствор хлороводорода в воде называют соляной (см. СОЛЯНАЯ КИСЛОТА) (хлороводородной) кислотой. Максимальная массовая концентрация соляной кислоты около 38%. Соли соляной кислоты - хлориды (см. ХЛОРИДЫ) , например, хлорид аммония NH4Cl, хлорид кальция СаСl2, хлорид бария ВаСl2 и другие. Многие хлориды хорошо растворимы в воде. Практически нерастворим в воде и в кислых водных растворах хлорид серебра AgCl. Качественная реакция на присутствие хлорид-ионов в растворе - образование с ионами Ag+ белого осадка AgСl, практически нерастворимого в азотнокислой среде:
СаСl2 + 2AgNO3 = Ca(NO3)2 + 2AgCl.
При комнатной температуре хлор реагирует с серой (образуется так называемая однохлористая сера S2Cl2) и фтором (образуются соединения ClF и СlF3). При нагревании хлор взаимодействует с фосфором (образуются, в зависимости от условий проведения реакции, соединения РСl3 или РСl5), мышьяком, бором и другими неметаллами. Непосредственно хлор не реагирует с кислородом, азотом, углеродом (многочисленные соединения хлора с этими элементами получают косвенными путями) и инертными газами (в последнее время ученые нашли способы активирования подобных реакций и их осуществления «напрямую»). С другими галогенами хлор образует межгалогенные соединения, например, очень сильные окислители - фториды ClF, ClF3, ClF5 . Окислительная способность хлора выше, чем брома, поэтому хлор вытесняет бромид-ион из растворов бромидов, например:
Cl2 + 2NaBr = Br2 + 2NaCl
Хлор вступает в реакции замещения со многими органическими соединениями, например, с метаном СН4 и бензолом С6Н6:
СН4+ Сl2 = СН3Сl + НСl или С6Н6 + Сl2 = С6Н5Сl + НСl.
Молекула хлора способна присоединятся по кратным связям (двойным и тройным) к органическим соединениям, например, к этилену С2Н4:
С2Н4 + Сl2 = СН2СlСН2Сl.
Хлор вступает во взаимодействие с водными растворами щелочей. Если реакция протекает при комнатной температуре, то образуются хлорид (например, хлорид калия КCl) и гипохлорит (см. ГИПОХЛОРИТЫ) (например, гипохлорит калия КClО):
Cl2 + 2КОН = КClО + КСl +Н2О.
При взаимодействии хлора с горячим (температура около 70-80°C) раствором щелочи образуется соответствующий хлорид и хлорат (см. ХЛОРАТЫ) , например:
3Сl2+ 6КОН= 5КСl + КСlО3+ 3Н2О.
При взаимодействии хлора с влажной кашицей из гидроксида кальция Са(ОН)2 образуется хлорная известь (см. ХЛОРНАЯ ИЗВЕСТЬ) («хлорка») СаСlОСl.
Степени окисления хлора +1 отвечает слабая малоустойчивая хлорноватистая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) НСlО. Ее соли - гипохлориты, например, NaClO - гипохлорит натрия. Гипохлориты - сильнейшие окислители, широко используются как отбеливающие и дезинфицирующие агенты. При взаимодействии гипохлоритов, в частности, хлорной извести, с углекислым газом СО2 образуется среди других продуктов летучая хлорноватистая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) , которая может разлагаться с выделением оксида хлора (I) Сl2О:
2НСlО = Сl2О + Н2О.
Именно запах этого газа Сl2О - характерный запах «хлорки».
Степени окисления хлора +3 отвечает малоустойчивая кислота средней силы НСlО2. Эту кислоту называют хлористой, ее соли - хлориты (см. ХЛОРИТЫ (соли)) , например, NaClO2 - хлорит натрия.
Степени окисления хлора +4 соответствует только одно соединение - диоксид хлора СlО2.
Степени окисления хлора +5 отвечает сильная, устойчивая только в водных растворах при концентрации ниже 40%, хлорноватая кислота (см. ХЛОРНОВАТИСТАЯ КИСЛОТА) НСlО3. Ее соли - хлораты, например, хлорат калия КСlО3.
Степени окисления хлора +6 соответствует только одно соединение - триоксид хлора СlО3 (существует в виде димера Сl2О6).
Степени окисления хлора +7 отвечает очень сильная и довольно устойчивая хлорная кислота (см. ХЛОРНАЯ КИСЛОТА) НСlО4. Ее соли - перхлораты (см. ПЕРХЛОРАТЫ) , например, перхлорат аммония NH4ClO4 или перхлорат калия КСlО4. Следует отметить, что перхлораты тяжелых щелочных металлов - калия, и особенно рубидия и цезия мало растворимы в воде. Оксид, соответствующий степени окисления хлора +7 - Сl2О7.
Среди соединений, содержащих хлор в положительных степенях окисления, наиболее сильными окислительными свойствами обладают гипохлориты. Для перхлоратов окислительные свойства нехарактерны.
Применение
Хлор - один из важнейших продуктов химической промышленности. Его мировое производство составляет десятки миллионов тонн в год. Хлор используют для получения дезинфицирующих и отбеливающих средств (гипохлорита натрия, хлорной извести и других), соляной кислоты, хлоридов многих металлов и неметаллов, многих пластмасс (поливинилхлорида (см. ПОЛИВИНИЛХЛОРИД) и других), хлорсодержащих растворителей (дихлорэтана СН2СlСН2Сl, четыреххлористого углерода ССl4 и др.), для вскрытия руд, разделения и очистки металлов и т.д. Хлор применяют для обеззараживания воды (хлорирования (см. ХЛОРИРОВАНИЕ) ) и для многих других целей.
Биологическая роль
Хлор относится к важнейшим биогенным элементам (см. БИОГЕННЫЕ ЭЛЕМЕНТЫ) и входит в состав всех живых организмов. Некоторые растения, так называемые галофиты, не только способны расти на сильно засоленных почвах, но и накапливают в больших количествах хлориды. Известны микроорганизмы (галобактерии и др.) и животные, обитающие в условиях высокой солености среды. Хлор - один из основных элементов водно-солевого обмена животных и человека, определяющих физико-химические процессы в тканях организма. Он участвует в поддержании кислотно-щелочного равновесия в тканях, осморегуляции (см. ОСМОРЕГУЛЯЦИЯ) (хлор - основное осмотически активное вещество крови, лимфы и др. жидкостей тела), находясь, в основном, вне клеток. У растений хлор принимает участие в окислительных реакциях и фотосинтезе.
Мышечная ткань человека содержит 0,20-0,52% хлора, костная - 0,09%; в крови - 2,89 г/л. В организме среднего человека (масса тела 70 кг) 95 г хлора. Ежедневно с пищей человек получает 3-6 г хлора, что с избытком покрывает потребность в этом элементе.
Особенности работы с хлором
Хлор - ядовитый удушливый газ, при попадании в легкие вызывает ожог легочной ткани, удушье. Раздражающее действие на дыхательные пути оказывает при концентрации в воздухе около 0,006 мг/л. Хлор был одним из первых химических отравляющих веществ (см. ОТРАВЛЯЮЩИЕ ВЕЩЕСТВА) , использованных Германией в Первую мировую войну. При работе с хлором следует пользоваться защитной спецодеждой, противогазом, перчатками. На короткое время защитить органы дыхания от попадания в них хлора можно тряпичной повязкой, смоченной раствором сульфита натрия Na2SO3 или тиосульфата натрия Na2S2O3. ПДК хлора в воздухе рабочих помещений 1 мг/м3, в воздухе населенных пунктов 0,03 мг/м3.
Полезные сервисы
фотосинтез
Энциклопедический словарь
ФОТОСИ́НТЕЗ [тэ], -а; м. Спец. Процесс образования углеводов из углекислоты и воды под действием света, поглощаемого хлорофиллом, в клетках зелёных растений, водорослей и некоторых микроорганизмов.
◁ Фотосинтети́ческий, -ая, -ое. Ф-ая деятельность. Ф-ая способность растений. Ф. аппарат живого листа. Ф-ие водоросли. Ф-ие слои воды.
* * *
фотоси́нтез (от фото... и синтез), превращение зелёными растениями и фотосинтезирующими микроорганизмами лучистой энергии Солнца в энергию химических связей органических веществ. Происходит с участием поглощающих свет пигментов (хлорофилл и др.). Суммарное выражение фотосинтеза у растений:
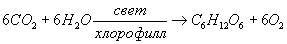 .
.
Фотосинтез - единственный биологический процесс, который идёт с увеличением свободной энергии и прямо или косвенно обеспечивает доступной химической энергией все земные организмы (кроме хемосинтезирующих). Ежегодно в результате фотосинтеза на Земле образуется около 150 млрд. т органического вещества, усваивается 300 млрд. т СО2 и выделяется около 200 млрд. т свободного О2. Благодаря фотосинтетической деятельности первых зелёных организмов в первичной атмосфере Земли появился кислород, возник озоновый экран, создались условия для биологической эволюции.
* * *
ФОТОСИНТЕЗ - ФОТОСИ́НТЕЗ, уникальный физико-химический процесс, осуществляемый на Земле всеми зелеными растениями и некоторыми бактериями и обеспечивающий преобразование электромагнитной энергии солнечных лучей в энергию химических связей различных органических соединений. Основа фотосинтеза - последовательная цепь окислительно-восстановительных реакций, в ходе которых осуществляется перенос электронов от донора - восстановителя (вода, водород) к акцептору - окислителю (СО2, ацетат) с образованием восстановленных соединений (углеводов) и выделением O2, если окисляется вода.
Фотосинтез играет ведущую роль в биосферных процессах, приводя в глобальных масштабах к образованию органического вещества из неорганического. Фотосинтезирующие организмы, используя солнечную энергию в реакциях фотосинтеза, осуществляют связь жизни на Земле со Вселенной и определяют в конечном итоге всю ее сложность и разнообразие. Гетеротрофные организмы - животные, грибы, большинство бактерий, а также бесхлорофилльные растения и водоросли - обязаны своим существованием автотрофным организмам - растениям-фотосинтетикам, создающим на Земле органическое вещество и восполняющим убыль кислорода в атмосфере. Человечество все более осознает очевидную истину, впервые научно обоснованную К.А. Тимирязевым (см. ТИМИРЯЗЕВ Климент Аркадьевич) и В.И. Вернадским (см. ВЕРНАДСКИЙ Владимир Иванович): экологическое благополучие биосферы и существование самого человечества зависит от состояния растительного покрова нашей планеты.
Фотосинтезирующие организмы
Самый примитивный тип фотосинтеза осуществляют галобактерии, живущие в средах с высоким (до30%) содержанием хлорида натрия. Простейшими организмами, способными осуществлять фотосинтез, являются также пурпурные и зеленые серобактерии (см. СЕРОБАКТЕРИИ), а также несерные пурпурные бактерии (см. ПУРПУРНЫЕ БАКТЕРИИ). Фотосинтетический аппарат этих организмов устроен гораздо проще (только одна фотосистема), чем у растений; кроме того, они не выделяют кислород, так как в качестве источника электронов используют соединения серы, а не воду. Фотосинтез такого типа получил название бактериального. Однако цианобактерии (прокариоты (см. ПРОКАРИОТЫ), способные к фоторазложению воды и выделению кислорода) обладают более сложной организацией фотосинтетического аппарата - двумя сопряженно работающими фотосистемами. У растений реакции фотосинтеза осуществляются в специализированной органелле клетки - хлоропласте. У всех растений (начиная от водорослей и мхов и кончая современными голосеменными и покрытосеменными) прослеживается общность в структурно-функциональной организации фотосинтетического аппарата.
Фотосинтетические пигменты
Основными пигментами, осуществляющими поглощение квантов света в процессе фотосинтеза, являются хлорофиллы (см. ХЛОРОФИЛЛ), пигменты Mg-порфириновой природы. Обнаружено несколько форм хлорофиллов, различающихся по химическому строению. Спектр поглощения различных форм хлорофиллов охватывает видимую, ближнюю ультрафиолетовую и ближнюю инфракрасную области спектра (у высших растений от 350 до 700 нм, а у бактерий - от 350 до 900 нм). Хлорофилл а является основным пигментом и характерен для всех организмов, осуществляющих оксигенный, т. е. с выделением кислорода, фотосинтез. У зеленых и эвгленовых водорослей, мхов и сосудистых растений, кроме хлорофилла a, имеется хлорофилл b, содержание которого составляет 1/4-1/5 от содержания хлорофилла a. Это дополнительный пигмент, расширяющий спектр поглощения света. У некоторых групп водорослей, в основном бурых и диатомовых, дополнительным пигментом служит хлорофилл с, а у красных водорослей - хлорофилл d.У пурпурных бактерий содержится бактериохлорофилл (см. БАКТЕРИОХЛОРОФИЛЛЫ)a и b, а у зеленых серных бактерий наряду с бактериохлорофиллом a содержатся бактериохлорофиллы c и d. В поглощении световой энергии участвуют и другие сопровождающие пигменты - каротиноиды (см. КАРОТИНОИДЫ)(пигменты полиизопреноидной природы) у фотосинтезирующих эукариот и фикобилины (пигменты с открытой тетрапиррольной структурой) у цианобактерий и красных водорослей. У галобактерий в плазматических мембранах обнаружен единственный пигмент - сложный белок бактериородопсин, близкий по химическому строению родопсину (см. РОДОПСИН) - зрительному пигменту сетчатки глаза.
В клетке молекулы хлорофилла находятся в различных агрегированных (связанных) состояниях и образуют пигмент-липопротеидные комплексы, и вместе с другими пигментами, участвующими в процессах поглощения квантов света и передачи энергии, связаны с белками фотосинтетических (тилакоидных) мембран, образуя так называемые светособирающие хлорофилл-белковые комплексы. По мере увеличения степени агрегации и плотности упаковки молекул максимум поглощения пигментов сдвигается в длинноволновую область спектра. Основная роль в поглощении световой энергии принадлежит коротковолновым формам, которые затем передают ее на более длинноволновые формы, участвующие в процессах миграции энергии. Присутствие в клетке серии спектрально близких форм пигментов обеспечивает высокую степень эффективности миграции энергии в реакционные фотохимические центры, где находятся наиболее длинноволновые формы пигментов, играющие роль так называемых энергетических ловушек.
Две стадии фотосинтеза
Процесс фотосинтеза состоит из двух последовательных и взаимосвязанных этапов: светового (фотохимического) и темнового (метаболического). На первой стадии происходит преобразование поглощенной фотосинтетическими пигментами энергии квантов света в энергию химических связей высокоэнергетического соединения АТФ и универсального восстановителя НАДФН - собственно первичных продуктов фотосинтеза, или так называемой «ассимиляционной силы». В темновых реакциях фотосинтеза происходит использование образовавшихся на свету АТФ и НАДФН в цикле фиксации углекислоты и ее последующего восстановления до углеводов.
У всех фотосинтезирующих организмов фотохимические процессы световой стадии фотосинтеза происходят в особых энергопреобразующих мембранах, называемых тилакоидными, и организованы в так называемую электрон-транспортную цепь. Темновые реакции фотосинтеза осуществляются вне тилакоидных мембран (в цитоплазме у прокариот и в строме хлоропласта у растений). Таким образом, световая и темновая стадии фотосинтеза разделены в пространстве и во времени.
Фотохимические реакции фотосинтеза. Общее представление о фотосистемах
Фотохимический этап фотосинтеза включает ряд последовательно протекающих процессов, локализованных в тилакоидных мембранах. Пигменты, специфически связанные с белками фотосинтетических мембран, и другие компоненты, необходимые для протекания реакций поглощения света и электронного транспорта, образуют надмолекулярные комплексы - фотосистему I (ФС I) и фотосистему II (ФС II). В составе каждой фотосистемы различают: реакционный центр, в котором происходят очень быстрые реакции первичного разделения зарядов; комплекс компонентов, по которым передается электрон от реакционного центра, и последний окисляется (электронтранспортная цепь); комплекс компонентов, за счет работы которых происходит фотоокисление воды и восстановление реакционного центра.
Первый этап сложного преобразования электромагнитного излучения (света) в свободную энергию химических связей включает поглощение фотонов светособирающими комплексами (антеннами), связанными с ФС I и ФС II (ССКI и ССКII, соответственно). Затем энергия возбуждения мигрирует по пигментам антенны (от более коротковолновых форм хлорофилла к более длинноволновым) и захватывается ловушкой - специализированным реакционным центром, который расположен в центре комплекса. Реакционные центры образованы самыми длинноволновыми формами хлорофилла а [с максимумом поглощения 700 нм (Р700) в ФС I и 680 нм (Р680) в ФС II]. Возбужденные Р700* и Р680* - очень сильные восстановители и быстро передают электрон на близко расположенную молекулу акцептора, а сами при этом окисляются. Эти реакции первичного разделения зарядов, происходящие в реакционных центрах ФС I и ФС II, являются единственными, в которых действительно происходит превращение энергии кванта света в химическую энергию. Дальнейший транспорт электронов, препятствующий рекомбинации зарядов, осуществляется по градиенту электрохимического потенциала компонентов электрон-транспортной цепи фотосинтеза.
Электронтранспортная цепь фотосинтеза и ее структурно-функциональная организация
Фотосинтетическую цепь переноса электронов, локализованную в тилакоидных мембранах, принято представлять в виде предложенной в 1961 так называемой «Z-схемы», в которой переносчики расположены по градиенту электрохимического потенциала. Свойства тилакоидной мембраны (высокое электрическое сопротивление, низкая проницаемость для ионов, анизотропная структура) обеспечивают, одновременно с переносом электронов по градиенту электрохимического потенциала, направленный трансмембранный перенос протонов (Н+) из стромы хлоропласта во внутритилакоидное пространство.
Местом локализации процесса фотосинтеза у эукариот являются специализированные органоиды клетки - хлоропласты, точнее их особые мембранные структуры - тилакоиды. Тилакоиды представляют собой уплощенные дисковидные полые мешки, в ограничивающих мембранах которых и осуществляется фотосинтез. Благодаря наличию многослойной системы тилакоидных мембран, отделяющих матрикс (строму) хлоропласта от внутреннего пространства тилакоида, пространство внутри хлоропластов строго структурировано. Тилакоиды могут либо находиться в тесном контакте друг с другом, образуя стопки (гранальные тилакоиды), либо обособленно располагаться в строме (стромальные тилакоиды). В липидном матриксе гранальных тилакоидных мембран локализована ФС II, стромальных - ФС I;. Белковый b/f-цитохромный комплекс локализован в тилакоидах обоих типов, а АТФ-синтазный комплекс - в стромальных тилакоидах и в соприкасающейся со стромой области гранальных тилакоидов.
Типы фотосинтетического транспорта электронов
ФС II осуществляет реакции фотоокисления воды, приводящие к образованию молекулярного кислорода и протона Н+. Светозависимый транспорт электронов от молекул воды через ФС II, b/f-цитохромный комплекс и ФС I к НАДФ+ носит название нециклического. Это основной (магистральный) путь переноса электронов в фотосинтетической цепи. Впервые выделение кислорода на свету в системе изолированных хлоропластов шпината с использованием искусственного акцептора электронов (феррицианида калия) наблюдал в 1939 английский исследователь Р. Хилл. Впоследствии нециклический перенос электронов (с участием физиологических или искусственных соединений), включающий работу обеих фотосистем или только одной из них получил название реакции Хилла.
Наряду с ним возможны так называемые альтернативные (дополнительные) пути: циклический и псевдоциклический. Циклический транспорт электронов осуществляется вокруг ФС I - in vivo он обычно включает пул пластохинонов, b/f-цитохромный комплекс и пластоцианин; in vitro (при использовании искусственных кофакторов) может осуществляться по более короткому пути. Циклический транспорт электронов (но со значительно меньшей скоростью) может осуществляться и вокруг ФС II.
Транспорт электронов называется псевдоциклическим, если вместо НАДФ+ акцептором электронов - от воды через ФС II, цитохром b/f-комплекс и компоненты восстановительной стороны ФС I - является молекулярный кислород. Кислород при этом либо не выделяется, либо наблюдается его видимое поглощение. Менее активен этот процесс в ФС II. При этом типе транспорта образуются высокореакционные восстановленный кислород - супероксид-анион-радикал O2- и пероксид водорода H2O2, которые обезвреживаются в хлоропласте с помощью фермента супероксиддисмутазы. Способность изолированных хлоропластов осуществлять фотовосстановление молекулярного кислорода впервые была показана немецким ученым А. Мелером в 1951. Впоследствии перенос электронов на молекулярный кислород (псевдоциклический транспорт электронов) получил название реакции Мелера.
Синтез АТФ и образование НАДФН
Одновременно с фотосинтетическим транспортом электронов происходит перенос протонов из стромы хлоропласта во внутритилакоидное пространство - возникает трансмембранный электрохимический градиент ионов водорода (pH-градиент), используемый затем комплексом фермента АТФ-синтазы для синтеза АТФ из АДФ и неорганического фосфата в процессе фотосинтетического фосфорилирования. При нециклическом токе электронов и сопряженном с ним фотофосфорилировании происходит образование восстановителя НАДФН и АТФ. При альтернативных путях переноса электронов - циклическом и псевдоциклическом - образуется только АТФ. Образующиеся в результате световых реакций первичные продукты фотосинтеза - НАДФН и АТФ - используются в ходе дальнейших ферментативных реакций для восстановления углекислоты до углеводов, жиров, белков. При неуглеводной направленности темнового метаболизма, когда преимущественно образуются аминокислоты, белки, органические кислоты, возрастает уровень потребления восстановителя НАДФН.
Темновые реакции фотосинтеза (фотосинтетическая фиксация CO 2 )
Метаболические варианты фотосинтетической фиксации CO2 у растений принято классифицировать на С3-, С4- и САМ-фотосинтез. Образующиеся в темновых реакциях углеводы могут откладываться в виде крахмала в хлоропластах; выходить из хлоропластов и использоваться в образовании нового структурного материала клеток; служить источником энергии для различных метаболических процессов; транспортироваться в запасающие органы растения.
С 3 -путь фотосинтеза
Восстановительный пентозофосфатный цикл фиксации CO2 (С3-путь, или цикл Кальвина), открытый американскими учеными Э. Бенсоном и М. Калвином (см. КАЛВИН Мелвин)в 1950-е годы, универсален и обнаруживается практически у всех автотрофных организмов. В этом цикле (рис.5) фиксация СО2 осуществляется на пятиуглеродное соединение рибулезобисфосфат (РуБФ) при участии фермента рибулезобисфосфаткарбоксилазы (РуБФ-карбоксилазы). Первым стабильным продуктом являются две молекулы трехуглеродного соединения 3-фосфоглицериновой кислоты (3-ФГК), восстанавливаемая затем с использованием АТФ и НАДФН до трехуглеводных сахаров, из которых образуется конечный продукт фотосинтеза - шестиуглеродная глюкоза. Субстратом ключевого фермента фотосинтетической фиксации СО2 - РуБФ-карбоксилазы - наряду с СО2 может быть и О2. При взаимодействии РуБФ с кислородом реализуется гликолатный, или С2-путь, известный как фотодыхание. Большинство наземных растений осуществляют фотосинтез по С3-пути. Типичные представители этой группы - горох, фасоль, конские бобы, шпинат, салат, капуста, пшеница, овес, рожь, ячмень, свекла, подсолнечник, тыква, томаты и другие одно- и двудольные растения.
С 4 -путь фотосинтеза
У некоторых видов растений (в основном тропических и очень небольшого числа видов из умеренных широт) первыми стабильными соединениями при фиксации СО2 являются четырехуглеродные органические кислоты - яблочная и аспарагиновая. Такие растения отличаются видимым отсутствием фотодыхания (или очень низким уровнем), высокой скоростью фиксации СО2 в расчете на единицу поверхности листа, более высокой общей фотосинтетической продуктивностью, быстрой скоростью роста. Функционально и анатомически в ткани их листьев выделяют 2 типа фотосинтезирующих клеток - клетки паренхимной обкладки, окружающие проводящие пучки, и клетки мезофилла.
Для всех растений этой группы характерна катализируемая ферментом фосфоенолпируваткарбоксилазой (ФЕП-карбоксилазой) фиксация СО2 на трехуглеродное соединение фосфоенолпируват (ФЕП) с образованием щавелевоуксусной кислоты, которая далее превращается в яблочную (малат) или аспарагиновую кислоту. Эти реакции протекают в цитоплазме клеток мезофилла листа. С4-кислоты затем поступают в клетки обкладки проводящих пучков, где подвергаются декарбоксилированию, а высвободившаяся СО2 фиксируется через цикл Кальвина. Следовательно, у С4-растений фотосинтетический метаболизм углерода пространственно разделен и осуществляется в клетках различного типа, т. е. по «кооперативному механизму», подробно описанному австралийскими исследователями М. Хетчем и К Слэком и советским биохимиком Ю. С. Карпиловым в конце 1960-1970 годов.
В соответствии с первичным механизмом декарбоксилирования С4-кислот все С4-растения подразделяются на три группы. НАДФ-малатдегидрогеназные растения осуществляют декарбоксилирование малата с помощью фермента НАДФ-малатдегидрогеназы в хлоропластах клеток обкладки проводящих пучков. Типичные представители этой группы - кукуруза, сахарный тростник, сорго, росичка кроваво-красная и другие злаки. НАД-малатдегидрогеназные растения осуществляют декарбоксилирование малата с помощью митохондриальной НАД-малатдегидрогеназы. Первичным продуктом фиксации углекислоты у них является аспартат. К типичным представителям этой группы принадлежат различные виды амаранта, портулак огородный, просо обыкновенное, бизонья трава, растущая в прериях Северной Америки и др. Фосфоенолпируват-карбоксикиназные растения осуществляют декарбоксилирование аспартата в цитоплазме клеток обкладки проводящих пучков с образованием ФЕП. Типичные представители - некоторые виды проса, хлориса, бутелуа.
У суккулентных растений, произрастающих в условиях водного дефицита, фиксация СО2 осуществляется с помощью так называемого САМ-пути (метаболизм кислот по типу растений семейства толстянковых). Первичный продукт фиксации углекислоты (яблочная кислота) образуется у них в темновой период и накапливается в вакуолях клеток листа. В дневное время при закрытых устьицах (которые закрываются для сохранения воды в тканях листа) осуществляется декарбоксилирование этой кислоты, а освобождающаяся СО2 поступает в цикл Кальвина.
Возникновение С4- и САМ-путей фотоассимиляции СО2 связано с давлением на высшие наземные растения засушливого климата. С4-растения хорошо адаптированы к высокой интенсивности света, повышенным температурам и засухе. Оптимальная температура для осуществления фотосинтеза у них выше, чем у С3-растений. С4-растения наиболее многочисленны в зонах с высокими температурами. Они более экономно используют воду по сравнению с С3-растениями. В настоящее время известно, что все растения с С4-фотосинтезом - цветковые (из 19 семейств:16 - двудольных и 3 -однодольных). Не обнаружено ни одного семейства, которое бы состояло только из С4-растений.
Генетика фотосинтеза
Хлоропласты обладают собственной системой синтеза РНК и белка. Они содержат двухцепочечную ДНК кольцеобразной формы, не связанную с гистонами, что роднит их с ДНК прокариот. ДНК хлоропластов кодирует рибосомную, транспортную и информационную РНК. Хлоропласты высокополиплоидны, т. е. каждый хлоропласт содержит много копий кольцевого генома, причем количество ДНК увеличивается по мере развития органеллы. Хлоропласты содержат рибосомы (см. РИБОСОМЫ) 70S и 20-30% общей РНК клетки. В процессе развития хлоропластов осуществляется считывание (транскрипция) как их собственного, так и ядерного геномов, что свидетельствует об их относительной автономности. Пластидная ДНК кодирует РНК рибосом, большую субъединицу РуБФ-карбоксилазы и специфические белки тилакоидов. Однако значительная часть хлоропластных белков кодируется ядерной ДНК, например, РНК-полимераза, малая субъединица РуБФ-карбоксилазы и др.
Экология фотосинтеза.
Интенсивность фотосинтеза зависит в первую очередь от интенсивности и спектрального состава света, концентрации СО2 и О2, температуры, водного режима растения, минерального питания и др. факторов внешней среды. Адаптация фотосинтеза к этим факторам лежит в основе жизнедеятельности растения. В условиях, когда внешние факторы не лимитируют скорость фотосинтеза, его интенсивность достигает максимальной величины и целиком определяется ростовой функцией. В среднем листья поглощают 80-85% энергии фотосинтетически активной радиации (400-700 нм) и 25% энергии инфракрасных лучей, что составляет около 55% общей солнечной радиации. Однако для фотосинтеза используется только 1,5-2% поглощенной энергии.
Зависимость скорости фотосинтеза от интенсивности падающего света имеет форму логарифмической кривой. У светолюбивых С3-растений максимальная скорость фотосинтеза наблюдается при освещении меньше яркого солнечного света. При дальнейшем увеличении интенсивности падающего света кривая скорости фотосинтеза постепенно выходит на плато (насыщение) и затем снижается (так называемое послеполуденное торможение). У С4-растений высокая скорость фотосинтеза наблюдается только при высоком уровне освещенности. У них отсутствует послеполуденное торможение фотосинтеза, а световая кривая не имеет насыщения на ярком солнечном свету.
При изменении условий освещения интенсивность фотосинтеза меняется, а фотосинтетический аппарат «настраивается» на новые условия на разных уровнях своей организации. Это важное адаптивное свойство позволяет растениям полнее использовать свет низких и умеренных интенсивностей и предохранять мембраны хлоропластов от повреждений при очень ярком свете, особенно если он сочетается с неблагоприятными факторами среды (низкой температурой, засухой и др.).
Качественный состав падающего света также влияет на скорость фотосинтеза и качественный состав его продуктов. Так, при выращивании растений на синем свету преимущественно образуются соединения неуглеводной природы - аминокислоты, белки и органические кислоты. Зависимость фотосинтеза от температуры описывается одновершинной кривой. У растений умеренного пояса интенсивность фотосинтеза достигает максимума в интервале температур 20-25°С и снижается при дальнейшем повышении температуры. При температуре 40°С фотосинтез практически полностью тормозится, а при 45°С такие растения погибают. Однако растения, произрастающие в пустыне, способны осуществлять фотосинтез даже при температуре 58°С. У растений северных широт нижняя температурная граница фотосинтеза находится в пределах от -15°С (сосна, ель) до -0,5°С, а у тропических растений - в области низких положительных температур (4-8°С).
Фотосинтез и урожай
Фотосинтетическая функция зеленого растения лежит в основе формирования урожая. Изучение закономерностей роста и развития растений, находящихся в тесной взаимосвязи с процессами фотосинтеза, минерального питания и водного режима растения, - основное направление селекционно-генетических и агротехнических работ, проводимых в мировой сельскохозяйственной практике. Оптимизация условий водоснабжения и минерального питания ведет, прежде всего, к увеличению суммарных размеров фотосинтетической поверхности посева - площади листьев, увеличению оптической и геометрической плотности посевов, и, следовательно, более полному использованию ими приходящей энергии солнечного света и углекислого газа из воздуха. До определенных пределов размер урожая находится в тесной связи с размерами площади листьев, длительностью и интенсивностью их работы. Однако по мере увеличения плотности посевов усиливается взаимное затенение листьев, снижается их освещенность, ухудшается вентиляция посевов, затрудняется поступление к листьям углекислого газа. В результате фотосинтетическая активность растения снижается. Обоснование мероприятий, направленных на усиление факторов, увеличивающих продуктивность растений, и на уменьшение и устранение условий, ограничивающих их продуктивность - главная задача разрабатываемой в нашей стране (А. А. Ничипорович (см. НИЧИПОРОВИЧ Анатолий Александрович), 1977) и за рубежом теории фотосинтетической продуктивности.
Фотосинтез и биосфера
Автотрофные растения Мирового океана (занимающего площадь около 360 млн. км2) по приблизительным подсчетам способны ежегодно превращать в органическое вещество 20-155 млрд. т углерода. При этом они используют всего 0,11% падающей на поверхность Земли солнечной энергии. Наземные растения (растущие на площади около 150 млн. км2) ежегодно фиксируют 16-24 млрд. т углерода. В результате фотосинтеза на земном шаре ежегодно образуется более 150 млрд. т углеводов. Кроме того, фотосинтез - единственный процесс, восполняющий убыль молекулярного кислорода из атмосферы в результате дыхания, горения и производственной деятельности человека. Ежегодная биопродукция О2 составляет около 100 млрд. т. Однако увеличивающееся с каждым годом промышленное потребление О2 достигает почти 5% от его биологической продукции. Ежегодный дефицит кислорода составляет почти 10 млрд. т. Одновременно регистрируется прирост СО2, ежегодно составляющий до 1,5% от содержания его в атмосфере. Однако некоторые исследователи считают, что при повышении СО2 в атмосфере скорость фотосинтеза увеличивается, что устраняет избыточное накопление углекислоты и восполняет убыль кислорода в атмосфере. Таким образом, в соответствии с основными функциями фотосинтеза можно выделить основные аспекты космической и планетарной роли зеленых растений: накопление органической массы; обеспечение постоянства содержания кислорода и СО2 в атмосфере; предохранение поверхности Земли от парникового эффекта; образование озонового экрана в верхних слоях атмосферы.
Краткая историческая справка
В истории исследований фотосинтеза выделяют несколько основных этапов. 1771-1850 гг. Открытие фотосинтеза английским ученым Дж. Пристли (см. ПРИСТЛИ Джозеф) и первые исследования по зависимости фотосинтеза от освещения, содержания хлорофилла в листе и наличия СО2в атмосфере (голландский врач Я. Ингенгауз и швейцарские естествоиспытатели Ж. Сенебье, Н. Соссюр (см. СОССЮР (естествоиспытатель, отец и сын))).
1850-1900 гг. Работы, связанные с исследованием энергетики фотосинтеза. Сформулированы основные положения о преобразовании в растении световой энергии в химическую (немецкий врач и физик Ю. Майер (см. МАЙЕР Юлиус Роберт)), о роли в этом процессе отдельных участков спектра (английский физик Д. Г. Стокс (см. СТОКС Джордж Габриель), немецкий ботаник Ю. Сакс). Исследованиями К. А. Тимирязева (см. ТИМИРЯЗЕВ Климент Аркадьевич) решен вопрос о зависимости фотосинтеза от лучей различной длины волны и сформулированы представления о фотосинтезе как процессе аккумуляции солнечной энергии.
1900-40 гг. Развитие физиологии фотосинтеза. В 1906 русский ботаник М. С. Цвет (см. ЦВЕТ Михаил Семенович) разработал метод хроматографического разделения и выделения хлорофиллов. Экспериментально обосновано представление о световых (фотохимических) и темновых (ферментативных) стадиях фотосинтеза (английский ученый Ф. Блекман, российский - А. А. Рихтер (см. РИХТЕР Андрей Александрович), немецкий - О. Варбург, американские - Р. Эмерсон, У. Арнольд). Английским исследователем Р. Хиллом в 1939 показано, что изолированные хлоропласты в присутствии искусственного акцептора электронов (феррицианида калия) способны осуществлять транспорт электронов от воды с выделением молекулярного кислорода.
1940-50 гг. На основании анализа распределения изотопов кислорода показано, что источником О2, выделяемого при фотосинтезе, является вода (российские ученые А. П. Виноградов и М. В. Тейц,1941).
1950-60 гг. Развитие биохимиии фотосинтеза. Обнаружение цитохромов в хлоропластах (Р. Хилл, 1951). М. Калвин, используя метод меченых атомов, выяснил путь углерода при фотосинтезе (Нобелевская премия по химии в 1961). Р. Эмерсон (1957) экспериментально обосновал концепцию о двух фотосистемах. Американский биохимик Д. Арнон открыл в 1954 фотосинтетическое фосфорилирование и провел различия между его циклическим и нециклическим путями. Разработаны основные положения фотохимии пигментов (российские ученые А. Н. Теренин, А. А. Красновский, американский биофизик Е. Рабинович и др.).
С 1960 по настоящее время. Развитие исследований в области биофизики, биохимии, молекулярной биологии, генетики и физиологии фотосинтеза. В 1960 Р. Хилл и Ф. Бендалл сформулировали представление о Z-схеме фотосинтеза. В 1966 М. Хетч и К. Слэк (и одновременно российский исследователь Ю. С. Карпилов) обнаружили путь С4-дикарбоновых кислот. В 70 гг. разработана теория фотосинтетической продуктивности растений (российский физиолог растений А. А. Ничипорович). Сформулированы представления о надмолекулярных комплексах ФС I, ФС II, bf-цитохромном и АТФ-синтазном комплексах и их локализации в тилакоидных мембранах хлоропластов. Установлена структура реакционного центра - основного компонента фотосинтетического аппарата у пурпурных бактерий (немецкие биофизики И. Дайзенхофер, Х. Михель и Р. Хубер; Нобелевская премия, 1988).