м.
Химический элемент, относящийся к лантаноидам; редкий металл, встречающийся в природе в соединениях.
м.
Химический элемент, относящийся к лантаноидам; редкий металл, встречающийся в природе в соединениях.
Ту́лий (лат. Thulium), химический элемент III группы периодической системы, относится к лантаноидам. Назван от греческого Thúlē - Туле. Металл. Плотность 9,318 г/см3; tпл 1545°C. Искусственно получаемый радиоактивный изотоп 170Tm - источник мягкого рентгеновского излучения.
* * *
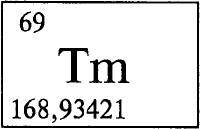
ТУЛИЙ - ТУ́ЛИЙ (лат. Thulium, у античных географов Thule - крайний север мира), Tm (читается «тулий»), химический элемент с атомным номером 69, атомная масса 168,93421, ранее химический символ был Tu. В природе встречается один стабильный изотоп 169Tm. Конфигурация трех внешних электронных слоев 4s2p6d10f135s2p6d06s2. Степени окисления +3, +2 (валентность III, II).
Расположен в группе IIIB в 6 периоде периодической системы элементов. Лантаноид (см. ЛАНТАНОИДЫ).
Радиус атома 0,174 нм, радиус ионов (координационное число 6) Тu3+ - 0,102 нм, Tu 2 +- 0,117 нм. Энергии последовательной ионизации 6,181, 12,05, 23,7, 42,7 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,1.
История открытия
Открыт в 1879 шведским химиком П. Т. Клеве (см. КЛЕВЕ Пьер Теодор), который выделил из минерала гадолинита оксид нового элемента. Идентифицировав элемент спектральным методом, Клеве назвал его в честь своей родины.
Нахождение в природе
Содержание в земной коре 2,7·10-5%. Входит в состав минералов: бастнезит (см. БАСТНЕЗИТ), монацит (см. МОНАЦИТ), лопарит (см. ЛОПАРИТ), ортит (см. ОРТИТ), ксенотим (см. КСЕНОТИМ).
Получение
Тулий концентрируется с иттербием (см. ИТТЕРБИЙ) и лютецием (см. ЛЮТЕЦИЙ). Разделение и очистку проводят методами ионной хроматографии или экстракции.
Металлический тулий получают металлотермическим восстановлением TmF3с использованием кальция (см. КАЛЬЦИЙ):
2TmF3+3Са=3СаF2+2Tm
или восстановлением Tm2O3металлическим лантаном (см. ЛАНТАН):
Tm2O3+La=La2O3+Tm
Физические и химические свойства
Тулий - мягкий серебристо-серый металл. Существует в одной модификации с гексагональной кристаллической решеткой типа Mg, а = 0,35375 нм, с = 0,55546 нм. Температура плавления 1545°C, кипения 1947°C, плотность 9,318 кг/дм3.
На воздухе компактный Tm устойчив. С галогенами (см. ГАЛОГЕНЫ) реагирует при нагревании, образуя TmF3 и TmCl3. Тулий взаимодействует с минеральными кислотами с образованием солей тулия(III). Сильными восстановителями Tm3+ восстанавливается до Tm2+.
Прокаливая на воздухе при 800-900°C нитрата Tm(NO3)3, оксалата Tm2(C2O4)3, сульфата Tm2(SO4)3 и других соединений Tm (III) образуется оксид тулия Tu2O3.
Применение
Тулий используют как активатор некоторых люминофоров и лазерных материалов, применяют при синтезе искусственных гранатов.
ТУЛИЙ (лат. Thulium) - Tm, химический элемент III группы периодической системы, атомный номер 69, атомная масса 168,9342, относится к лантаноидам. Название от греч. Thule - Туле. Металл. Плотность 9,318 г/см³, tпл 1545 .С. Искусственно получаемый радиоактивный изотоп 170Tm - источник мягкого рентгеновского излучения.
ТУЛИЙ (Tulium), Tm, химический элемент III группы периодической системы, атомный номер 69, атомная масса 168,9342; относится к редкоземельным элементам; металл. Открыт шведским химиком П. Клеве в 1879.
ту́лий
(лат. thule полулегендарная страна, в древности считавшаяся северной оконечностью земли) хим. элемент из семейства лантаноидов, символ Tm (лат. thulium), металл.
- Химический элемент, получивший своё название от старого латинского обозначения скандинавских стран.
- Редкоземельный металл.
- Химический элемент, Tm.