прил., кол-во синонимов: 2
сублимирование
Толковый словарь
I ср.
процесс действия по несов. гл. сублимировать I
II ср.
процесс действия по несов. гл. сублимировать II
Энциклопедический словарь
Орфографический словарь
Синонимы к слову сублимирование
Словарь галлицизмов русского языка
СУБЛИМИРОВАНИЕ я, ср. sublimer, нем. sublimieren <лат. sublimare высоко поднимать; возносить. хим. Алюдели употребляются для собрания и удержания сухих и летучих веществ, кои желают превратить в цветы субимированием. Ян. 1803.
Полезные сервисы
сублимированный
Толковый словарь Ушакова
СУБЛИМИ́РОВАННЫЙ, сублимированная, сублимированное (хим.). прич. страд. прош. вр. от сублимировать.
Энциклопедический словарь
Орфографический словарь
Словарь ударений
Синонимы к слову сублимированный
Морфемно-орфографический словарь
Полезные сервисы
сублимировать
Толковый словарь
I несов. и сов.; перех.
Производить сублимацию [сублимация I].
II несов. и сов.; перех.
Осуществлять сублимацию [сублимация II].
Толковый словарь Ушакова
СУБЛИМИ́РОВАТЬ, сублимирую, сублимируешь, совер. и несовер., что (от лат. sublimo-возношу) (хим.). Произвести (производить) сублимацию.
Толковый словарь Даля
СУБЛИМИРОВАТЬ - и сублимовать лат., хим. возгонять огнем, гнать сухою перегонкой, -ся, возгоняться, перегоняться химически; сублимат, субламация, действие по гл.
| перегон, что перегнано. Из сублимат сделано сулема, перегон ртути.
Энциклопедический словарь
СУБЛИМИ́РОВАТЬ -рую, -руешь; св. и нсв. Спец.
1. что. Произвести - производить сублимацию. С. серу. С. йод.
2. Претерпеть - претерпевать сублимацию. Вещества, сублимирующие при высоких температурах.
3. Произвести - производить сублимацию (2 зн.). С. любовную энергию на творческий труд.
◁ Сублими́роваться, -руется; нсв. (1, 3 зн.). Сублими́рование, -я; ср.
Академический словарь
-рую, -руешь; сов. и несов. хим.
1. перех.
Произвести (производить) сублимацию.
2. Претерпеть (претерпевать) сублимацию.
Вещества, сублимирующие при высоких температурах.
Орфографический словарь
Грамматический словарь
Словарь галлицизмов русского языка
СУБЛИМИРОВАТЬ sublimer, нем. sublimieren <, лат. sublimo. хим. Производить сублимацию. Уш. 1940. Сублимировать серу. Сублимировать йод. БАС-1.
2. Претерпевать сублимацию. Вещества, сублимирующие при высоких температурах. БАС-1. | перен. Сублимируючи похоть, редуцируючи страх, Я приветсвую эпохи В резвоскачущих стихах. Т. Кибирев. // Знамя 2002 1 3. - Лекс. Ян. 1806: сублимированный; САН 1847: сублими/ровать; Рейф 1877: сублими/ровать и сублимо/вать.
Словарь иностранных слов
сублимировать
- рую, рует, несов. и сов., что (нем. sublimieren < лат. - см. сублимация).
1. тех. Производить (произвести) сублимацию. С. лед в пар.
2. мед. Осуществлять (осуществить) сублимацию. С. сексуальную энергию в интеллектуальное творчество.
Сублимирование - действие по глаголу с. 1, 2.
Полезные сервисы
сублимироваться
Толковый словарь
I несов. неперех.
страд. к несов. гл. сублимировать I
II несов. неперех.
страд. к несов. гл. сублимировать II
Толковый словарь Ушакова
СУБЛИМИ́РОВАТЬСЯ, сублимируюсь, сублимируешься, несовер. (хим.). страд. к сублимировать.
Академический словарь
Орфографический словарь
Формы слов для слова сублимироваться
сублими́роваться, сублими́руюсь, сублими́руемся, сублими́руешься, сублими́руетесь, сублими́руется, сублими́руются, сублими́руясь, сублими́ровался, сублими́ровалась, сублими́ровалось, сублими́ровались, сублими́руйся, сублими́руйтесь, сублими́рующийся, сублими́рующаяся, сублими́рующееся, сублими́рующиеся, сублими́рующегося, сублими́рующейся, сублими́рующихся, сублими́рующемуся, сублими́рующимся, сублими́рующуюся, сублими́рующеюся, сублими́рующимися, сублими́рующемся, сублими́ровавшийся, сублими́ровавшаяся, сублими́ровавшееся, сублими́ровавшиеся, сублими́ровавшегося, сублими́ровавшейся, сублими́ровавшихся, сублими́ровавшемуся, сублими́ровавшимся, сублими́ровавшуюся, сублими́ровавшеюся, сублими́ровавшимися, сублими́ровавшемся
Грамматический словарь
Словарь галлицизмов русского языка
СУБЛИМИРОВАТЬСЯ sublimer, нем. sublimieren <, лат. sublimo.
1. хим. Подвергаться сублимации.
2. перен. Его <поленова> собственный живописный стиль, импрессионизм его станковых работ, в декорации сублимировался в декоративизм. НН 1998 46 130. - Лекс. САН 1847: сублими/роваться.
Полезные сервисы
углерода диоксид
Энциклопедия Кольера
УГЛЕРОДА ДИОКСИД (оксид углерода(IV), ангидрид угольной кислоты, углекислый газ) CO2, хорошо известный пузырящийся ингредиент газированных безалкогольных напитков. Человек знал о целебных свойствах "шипучей воды" из природных источников с незапамятных времен, но только в 19 в. научился получать ее сам. Тогда же было идентифицировано вещество, делающее воду шипучей, - углекислый газ. Впервые для целей карбонизации этот газ был получен в 1887 в ходе реакции между измельченным мрамором и серной кислотой; его выделяли и из природных источников. Позже СО2 стали получать в промышленных масштабах сжиганием кокса, прокаливанием известняка и брожением спирта. Более четверти века диоксид углерода хранили в стальных баллонах под давлением и использовали почти исключительно для газирования напитков. В 1923 как коммерческий продукт стали производить твердый СО2 (сухой лед), а примерно в 1940 - жидкий, который разливали в специальные герметичные цистерны под высоким давлением.
Физические свойства. При обычных температуре и давлении диоксид углерода - бесцветный, обладающий слегка кисловатым вкусом и запахом газ. Он на 50% тяжелее воздуха, поэтому его можно переливать из одной емкости в другую. СО2 - продукт большинства процессов горения и при достаточно больших количествах может гасить пламя, вытесняя из воздуха кислород. При увеличении концентрации СО2 в плохо проветриваемом помещении содержание кислорода в воздухе уменьшается настолько, что человек может задохнуться. СО2 растворяется во многих жидкостях; растворимость зависит от свойств жидкости, температуры и давления паров СО2. Способность диоксида углерода растворяться в воде и определяет его широкое использование в производстве безалкогольных напитков. СО2 прекрасно растворяется в органических растворителях, например в спирте, ацетоне и бензоле. При повышении давления и охлаждении диоксид углерода легко сжижается и находится в жидком состоянии при температурах от +31 до -57° С (в зависимости от давления). Ниже -57° С переходит в твердое состояние (сухой лед). Давление, необходимое для сжижения, зависит от температуры: при +21° С оно составляет 60 атм, а при -18° С всего 20 атм. Жидкий СО2 хранят в герметичных емкостях под соответствующим давлением. При переходе в атмосферу часть его превращается в газ, а некоторое количество - в "углеродный снег", при этом его температура понижается до -84° С. Поглощая тепло из окружающей среды, сухой лед переходит в газообразное состояние, минуя жидкую фазу, - сублимирует. Для уменьшения сублимационных потерь его хранят и транспортируют в герметичных контейнерах, достаточно прочных, чтобы выдержать увеличение давления при повышении температуры.
Химические свойства. СО2 - малоактивное соединение. При растворении в воде образует слабую угольную кислоту, окрашивающую лакмусовую бумажку в красный цвет. Угольная кислота улучшает вкусовые качества газированных напитков и предотвращает рост бактерий. Реагируя со щелочными и щелочноземельными металлами, а также с аммиаком, СО2 образует карбонаты и бикарбонаты.
См. также УГЛЕРОД. Распространенность в природе и получение. СО2 образуется при сжигании углеродсодержащих веществ, спиртовом брожении, гниении растительных и животных остатков; он высвобождается при дыхании животных, его выделяют растения в темноте. На свету, напротив, растения поглощают СО2 и выделяют кислород, что поддерживает природный баланс кислорода и углекислого газа в воздухе, которым мы дышим. Содержание СО2 в нем не превышает 0,03% (по объему). Известно пять основных способов получения СО2: сжигание углеродсодержащих веществ (кокса, природного газа, жидкого топлива); образование в качестве побочного продукта при синтезе аммиака; прокаливание известняка; брожение; откачка из скважин. В последних двух случаях получается практически чистый диоксид углерода, а при сжигании углеродсодержащих веществ или прокаливании известняка образуется смесь СО2 с азотом и следами других газов. Эту смесь пропускают через раствор, поглощающий только СО2. Затем раствор нагревают и получают практически чистый СО2, который отделяют от оставшихся примесей. От паров воды избавляются вымораживанием и химической сушкой. Очищенный СО2 сжижают, охлаждая его при высоком давлении, и хранят в больших емкостях. Для получения сухого льда жидкий СО2 подают в закрытую камеру гидравлического пресса, где понижают давление до атмосферного. При резком снижении давления из СО2 образуются рыхлый снег и очень холодный газ. Снег прессуют и получают сухой лед. Газообразный СО2 откачивают, сжижают и возвращают в резервуар для хранения.
ПРИМЕНЕНИЕ
Получение низких температур. В жидком и твердом виде СО2 применяется в основном как хладагент. Сухой лед - компактный материал, удобный в обращении и позволяющий создавать разные температурные режимы. При той же массе он превосходит обычный лед по хладоемкости более чем в два раза, занимая вдвое меньший объем. Сухой лед используется при хранении пищевых продуктов. Им охлаждают шампанское, безалкогольные напитки и мороженое. Он широко применяется при "холодном измельчении" термочувствительных материалов (мясных продуктов, смол, полимеров, красителей, инсектицидов, красок, приправ); при галтовке (очистке от заусенцев) штампованных изделий из резины и пластика; при низкотемпературных испытаниях летательных аппаратов и электронных устройств в специальных камерах; для "холодного смешивания" полуфабрикатов кексов и тортов, чтобы при выпечке они сохраняли однородность; для быстрого охлаждения контейнеров с транспортируемыми продуктами обдуванием их струей измельченного сухого льда; при закалке легированных и нержавеющих сталей, алюминия и т.д. с целью улучшения их физических свойств; для плотной посадки деталей машин при их сборке; для охлаждения резцов при обработке высокопрочных стальных заготовок.
Карбонизация. Основное применение газообразного СО2 - карбонизация воды и безалкогольных напитков. Вначале воду и сироп смешивают в нужных пропорциях, а затем под давлением насыщают смесь газообразным СО2. Карбонизация пива и вин обычно происходит в результате протекающих в них химических реакций. Применения, основанные на инертности. СО2 применяется как антиоксидант при долговременном хранении многих пищевых продуктов: сыра, мяса, сухого молока, орехов, растворимых чая, кофе, какао и т.д. Как вещество, подавляющее горение, СО2 используют при хранении и транспортировке горючих материалов, например ракетного топлива, масел, бензина, красок, лаков, растворителей. Он используется как защитная среда при электросварке углеродистых сталей с целью получения однородного прочного шва, при этом сварочные работы оказываются дешевле, чем при использовании инертных газов. СО2 - одно из наиболее эффективных средств тушения пожаров, возникающих при воспламенении горючих жидкостей и электрических пробоях. Выпускают разные углекислотные огнетушители: от портативных емкостью не более 2 кг до стационарных установок автоматической подачи с общей емкостью баллонов до 45 кг или газовых резервуаров низкого давления емкостью до 60 т СО2. Жидкий СО2, находящийся в таких огнетушителях под давлением, при выпуске образует смесь из снега и холодного газа; последний обладает большей плотностью, чем воздух, и вытесняет его из зоны горения. Эффект усиливается еще и охлаждающим действием снега, который, испаряясь, переходит в газообразный СО2.
Химические аспекты. Диоксид углерода применяется в производстве аспирина, свинцовых белил, мочевины, перборатов, химически чистых карбонатов. Угольная кислота, образующаяся при растворении СО2 в воде, - недорогой реагент для нейтрализации щелочей. В литейном производстве при помощи диоксида углерода отверждают песочные формы благодаря взаимодействию CO2 с силикатом натрия, смешанным с песком. Это позволяет получать более качественные отливки. Огнеупорный кирпич, которым выложены печи для выплавки стали, стекла и алюминия, после обработки диоксидом углерода становится более прочным. СО2 используется также в городских системах умягчения воды с помощью натронной извести.
Создание повышенного давления. СО2 применяют для опрессовки и проверки на течь различных емкостей, а также для калибровки манометров, клапанов, свечей зажигания. Им наполняют портативные контейнеры для накачивания спасательных поясов и надувных лодок. Смесь диоксида углерода и закиси азота долгое время применяли для создания давления в аэрозольных баллончиках. СО2 нагнетают под давлением в герметичные емкости с эфиром (в устройствах для быстрого запуска двигателей), растворителями, красками, инсектицидами для последующего распыления этих веществ.
Применение в медицине. В небольших количествах СО2 добавляют к кислороду (для стимуляции дыхания) и при анестезии. В высоких концентрациях его применяют для гуманного умерщвления животных.
ЛИТЕРАТУРА
Реми Г. Курс неорганической химии, т. 1. М., 1972 Некрасов Б.В. Основы общей химии. М., 1973
Полезные сервисы
мышьяк
Энциклопедический словарь
МЫШЬЯ́К -а́; м.
1. Химический элемент (Аs) - твёрдое ядовитое вещество блестяще-серого цвета, входящее в состав многих минералов. Окисел мышьяка. Получение мышьяка.
2. Лекарственный препарат, содержащий это вещество или его соединения (применяется как общеукрепляющее, противомикробное и т.п. средство). Лечение мышьяком. Воздействие мышьяка на нервные окончания.
◁ Мышьяко́вый, -ая, -ое. М-ые соединения. М-ая кислота. М. препарат. М-ое отравление. Мышья́чный, -ая, -ое. Устар. Мышьяко́вистый, -ая, -ое. ● Русское название этого элемента произошло от слова "мышь", т.к. мышьяк широко применялся при уничтожении крыс и мышей.
* * *
мышья́к (лат. Arsenicum), химический элемент V группы периодической системы. Русское название от «мышь» (препараты мышьяка применялись для истребления мышей и крыс). Образует несколько модификаций. Обычный мышьяк (так называемый металлический, или серый) - хрупкие кристаллы с серебристым блеском; плотность 5,74 г/см3, при 615°C возгоняется. На воздухе окисляется и тускнеет. Добывают из сульфидных руд (минералы арсенопирит, аурипигмент, реальгар). Компонент сплавов с медью, свинцом, оловом и др. и полупроводниковых материалов. Соединения мышьяка физиологически активны и ядовиты; служили одними из первых инсектицидов (см., например, Арсенаты металлов). Неорганические соединения мышьяка применяются в медицине как общеукрепляющие, тонизирующие средства, органические - как противомикробные и противопротозойные (при лечении сифилиса, амёбиаза и др.).
* * *
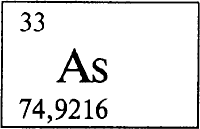
МЫШЬЯК - МЫШЬЯ́К (лат. Arsenicum, от греческого arsen - сильный), As (читается «арсеникум»), химический элемент c атомным номером 33, атомная масса 74,9216. В природе встречается один стабильный изотоп 75As. Расположен в VА группе в 4 периоде периодической системы элементов. Электронная конфигурация внешнего слоя 4s2p3. Степени окисления +3, +5, -3 (валентности III, V).
Радиус атома 0,148 нм. Радиус иона Аs3- 0,191 нм, иона As3+ 0,072 нм (координационное число 4), иона As5+0,047 нм (6). Энергии последовательной ионизации 9,82, 18,62, 28,35, 50,1 и 62,6 эВ. электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 2,1. Неметалл.
Историческая справка
Мышьяк известен человечеству с древнейших времен, когда использовались в качестве красителей минералы аурипигмент (см. АУРИПИГМЕНТ) As2S3и реальгар (см. РЕАЛЬГАР)As 4S 4(упоминания о них встречаются у Аристотеля) (см. АРИСТОТЕЛЬ).
Алхимики при прокаливании сульфидов мышьяка на воздухе отмечали, что образование так называемого белого оксида As 2O3:
2As 2S3+9О2=2As2O3+6SO2
Этот оксид - сильный яд, он растворяется в воде и в вине.
Впервые As в свободном виде получил немецкий алхимик А. фон Больдштндт в 13 веке прогреванием оксида мышьяка с углем:
As2O3 +3С=2As+3СО
Для изображения мышьяка использовали знак извивающейся змеи с раскрытой пастью.
Нахождение в природе
Мышьяк - рассеянный элемент. Содержание в земной коре 1,7·10-4% по массе. Известно 160 мышьяксодержащих минералов. В самородном состоянии встречается редко. Минерал, имеющий промышленное значение - арсенопирит (см. АРСЕНОПИРИТ) FeAsS. As часто содержится в свинцовых, медных и серебряных рудах.
Получение
Обогащенную руду подвергают окислительному обжигу, затем сублимируют летучий As2O3.. Этот оксид восстанавливают углеродом. Для очистки As его подвергают дистилляции в вакууме, затем переводят в летучий хлорид AsCl3, который восстанавливают водородом (см. ВОДОРОД). Получаемый мышьяк содержит 10-5-10-6% примесей по массе.
Физические и химические свойства
Мышьяк - серое с металлическим блеском хрупкое вещество (a-мышьяк) с ромбоэдрической кристаллической решеткой, a = 0,4135 нм и a = 54,13°. Плотность 5,74 кг/дм3.
При нагревании до 600°C As сублимирует. При охлаждении паров возникает новая модификация - желтый мышьяк. Выше 270°C все формы As переходят в черный мышьяк.
Расплавить As можно только в запаянных ампулах под давлением. Температура плавления 817°C при давлении его насыщенных паров 3,6МПа.
Структура серого мышьяка похожа на структуру серой сурьмы и по строению напоминает черный фосфор.
Мышьяк химически активен. При хранении на воздухе порошкообразный As воспламеняется с образованием кислотного оксида As2O3. Этот оксид в парах существует в виде димеров As4O6.
При осторожном обезвоживании мышьяковой кислоты H3AsO4 получают высший кислотный оксид мышьяка As2O5, который при нагревании легко отдает кислород (см. КИСЛОРОД), превращаясь в As2O3.
Оксиду As2O3 отвечают существующие только в растворах ортомышьяковистая H3AsO3 и метамышьяковистая слабые кислоты HAsO2. Их соли - арсенаты.
Разбавленная азотная кислота (см. АЗОТНАЯ КИСЛОТА) окисляет As до H3AsO3, концентрированная азотная кислота - до H3AsO4. Со щелочами As не реагирует, в воде растворяется.
При нагревании As и H2образуется газ арсин (см. МЫШЬЯКА ГИДРИД) AsH3. С фтором (см. ФТОР) и хлором (см. ХЛОР) As взаимодействует с самовоспламенением. При взаимодействии As с серой (см. СЕРА), селеном (см. СЕЛЕН) и теллуром (см. ТЕЛЛУР) образуются хальгкогениды: (см. ХАЛЬКОГЕНИДЫ) As2S5, As2S3, As4S4, As2Se3, As2Te3, существующие в стеклообразном состоянии. Они являются полупроводниками.
Со многими металлами As образует арсениды (см. АРСЕНИДЫ). Арсенид галлия GaAs и индия InAs - полупроводники (см. ПОЛУПРОВОДНИКИ).
Известно большое число органических соединений мышьяка, в которых имеется химическая связь As - C: органоарсины RnAsH3-n (n = 1,3), тетраорганодиарсины R2As - AsR2 и другие.
Применение
As особой чистоты используется для синтеза полупроводниковых материалов. Иногда As добавляют к сталям как легирующую добавку.
В 1909 немецкий микробиолог П. Эрлих (см. ЭРЛИХ Пауль) получил «препарат 606», эффективное лекарство от малярии, сифилиса, возвратного тифа.
Физиологическое действие
Мышьяк и все его соединения ядовиты. При остром отравлении мышьяком наблюдаются рвота, боли в животе, понос, угнетение центральной нервной системы. Помощь и противоядия при отравлении мышьяком: прием водных растворов Na2S2O3. Промывание желудка, прием молока и творога; специфическое противоядие - унитиол. ПДК в воздухе для мышьяка 0,5мг/м3. Работают с мышьяком в герметичных боксах, используя защитную спецодежду. Из-за высокой токсичности соединения мышьяка использовались Германией как отравляющие вещества в Первую мировую войну.
На территориях, где в почве и воде избыток мышьяка, он накапливается в щитовидной железе у людей и вызывает эндемический зоб.
Полезные сервисы
углерод
Энциклопедический словарь
УГЛЕРО́Д -а; м. Химический элемент (C), важнейшая составная часть всех органических веществ в природе. Атомы углерода. Процент содержания углерода. Без углерода невозможна жизнь.
◁ Углеро́дный, -ая, -ое. У-ые атомы. Углеро́дистый, -ая, -ое. Содержащий углерод. У-ая сталь.
* * *
углеро́д (лат. Carboneum), химический элемент IV группы периодической системы. Основные кристаллические модификации - алмаз и графит. При обычных условиях углерод химически инертен; при высоких температурах соединяется со многими элементами (сильный восстановитель). Содержание углерода в земной коре 6,5·1016 т. Значительное количество углерода (около 1013 т) входит в состав горючих ископаемых (уголь, природный газ, нефть и др.), а также в состав углекислого газа атмосферы (6·1011 т) и гидросферы (1014 т). Главные углеродсодержащие минералы - карбонаты.
Углерод обладает уникальной способностью образовывать огромное количество соединений, которые могут состоять практически из неограниченного числа атомов углерода. Многообразие соединений углерода определило возникновение одного из основных разделов химии - органической химии.
Углерод - биогенный элемент; его соединения играют особую роль в жизнедеятельности растительных и животных организмов (среднее содержание углерода - 18%). Углерод широко распространён в космосе; на Солнце он занимает 4-е место после водорода, гелия и кислорода.

* * *
УГЛЕРОД - УГЛЕРО́Д (лат. Carboneum, от cаrbo - уголь), С (читается «це»), химический элемент с атомным номером 6, атомная масса 12,011. Природный углерод состоит из двух стабильных нуклидов: 12С, 98,892% по массе и 13C - 1,108%. В природной смеси нуклидов в ничтожных количествах всегда присутствует радиоактивный нуклид 14C (b--излучатель, период полураспада 5730 лет). Он постоянно образуется в нижних слоях атмосферы при действии нейтронов космического излучения на изотоп азота 14N:
147N + 10n = 146C + 11H.
Углерод расположен в группе IVA, во втором периоде периодической системы. Конфигурация внешнего электронного слоя атома в основном состоянии 2s2p2. Важнейшие степени окисления +2 +4, -4, валентности IV и II.
Радиус нейтрального атома углерода 0,077 нм. Радиус иона C4+ 0,029 нм (координационное число 4), 0,030 нм (координационное число 6). Энергии последовательной ионизации нейтрального атома равны 11,260, 24,382, 47,883, 64,492 и 392,09 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 2,5.
Историческая справка
Углерод известен с глубокой древности. Древесный уголь использовали для восстановления металлов из руд, алмаз (см. АЛМАЗ (минерал)) - как драгоценный камень. В 1789 французский химик А. Л. Лавуазье (см. ЛАВУАЗЬЕ Антуан Лоран) сделал вывод об элементарной природе углерода.
Искусственные алмазы впервые были получены в 1953 шведскими исследователями, но результаты они не успели опубликовать. В декабре 1954 искусственные алмазы получили, а в начале 1955 опубликовали результаты сотрудники компании «Дженерал электрик». (см. ДЖЕНЕРАЛ ЭЛЕКТРИК)
В СССР искусственные алмазы впервые были получены в 1960 группой ученых под руководством В. Н. Бакуля и Л. Ф. Верещагина (см. ВЕРЕЩАГИН Леонид Федорович) .
В 1961 группой советских химиков под руководством В. В. Коршака была синтезирована линейная модификация углерода - карбин. Вскоре карбин был обнаружен в метеоритном кратере Рис (Германия). В 1969 в СССР были синтезированы нитевидные кристаллы алмаза при обычном давлении, обладающие высокой прочностью и практически лишенные дефектов.
В 1985 Г. Крото (см. КРОТО Гаролд) обнаружил новую форму углерода -фуллерены (см. ФУЛЛЕРЕНЫ)С60 и С70 в масс-спектре испаряемого при облучении лазером графита. При высоких давлениях получен лонсдейлит.
Нахождение в природе
Содержание в земной коре 0,48% по массе. Накапливается в биосфере: в живом веществе 18% угля, в древесине 50%, торфе 62%, природных горючих газах 75%, горючих сланцах 78%, каменном и буром угле 80%, нефти 85%, антраците 96%. Значительная часть угля литосферы сосредоточена в известняках и доломитах. Углерод в степени окисления +4 входит в состав карбонатных пород и минералов (мел, известняк, мрамор, доломиты). Углекислый газ CO2 (0,046% по массе) постоянный компонент атмосферного воздуха. Углекислый газ в растворенном виде всегда присутствует в воде рек, озер и морей.
В атмосфере звезд, планет и в метеоритах обнаружены вещества, содержащие углерод.
Получение
С древности уголь получали при неполном сгорании древесины. В 19 веке древесный уголь в металлургии заменили каменным углем (коксом).
В настоящее время для промышленного получения чистого углерода используют крекинг (см. КРЕКИНГ) природного газа метана (см. МЕТАН) СН4:
СН4 = С + 2Н2
Уголь для медицинских целей готовят сжиганием кожуры кокосовых орехов. Для лабораторных нужд чистый уголь, не содержащий несгораемых примесей, получают неполным сжиганием сахара.
Физические и химические свойства
Углерод - неметалл.
Многообразие соединений углерода объясняется способностью его атомов связываться между собой, образуя объемные структуры, слои, цепи, циклы. Известны четыре аллотропические модификации углерода: алмаз, графит, карбин и фуллерит. Древесный уголь состоит из мельчайших кристалликов с неупорядоченной структурой графита. Его плотность 1,8-2,1 г/см3 . Сажа представляет собой сильно измельченный графит.
Алмаз - минерал с кубической гранецентрированной решеткой. Атомы С в алмазе находятся в sp3-гибридизованном состоянии. Каждый атом образует 4 ковалентные s-связи с четырьмя соседними атомами С, расположенными по вершинам тетраэдра, в центре которого находится атом С. Расстояния между атомами в тетраэдре 0,154 нм. Электронная проводимость отсутствует, ширина запрещенной зоны 5,7 эВ. Из всех простых веществ алмаз имеет максимальное число атомов, приходящихся на единицу объема. Его плотность 3,51 г/см3.. Твердость по минералогической шкале Мооса (см. МООСА ШКАЛА) принята за 10. Алмаз можно поцарапать только другим алмазом; но он хрупок и при ударе раскалывается на куски неправильной формы. Термодинамически устойчив лишь при высоких давлениях. Однако, при 1800 °C превращение алмаза в графит происходит быстро. Обратное превращение графита в алмаз происходит при 2700°C и давлении 11-12 ГПа.
Графит - слоистое темно-серое вещество с гексагональной кристаллической решеткой. Термодинамически устойчив в широком интервале температур и давлений. Состоит из параллельных слоев, образованных правильными шестиугольниками из атомов С. Углеродные атомы каждого слоя расположены против центров шестиугольников, находящихся в соседних слоях; положение слоев повторяется через один, а каждый слой сдвинут относительно другого в горизонтальном направлении на 0,1418 нм. Внутри слоя связи между атомами ковалентные, образованы sp2-гибридными орбиталями. Связи между слоями осуществляются слабыми ван-дер-ваальсовыми (см. МЕЖМОЛЕКУЛЯРНОЕ ВЗАИМОДЕЙСТВИЕ) силами, поэтому графит легко расслаивается. Такое состояние стабилизирует четвертая делокализованная p-связь. Графит обладает хорошей электрической проводимостью. Плотность графита 2,1-2,5 кг/дм3.
Во всех аллотропических модификациях при обычных условиях углерод химически малоактивен. В химические реакции вступает только при нагревании. При этом химическая активность углерода убывает в ряду сажа-древесный уголь-графит-алмаз. Сажа на воздухе воспламеняется при нагревании до 300°C, алмаз - при 850-1000°C. При горении образуется углекислый газ СО2 и CO. Нагревая СО2 с углем, также получают оксид углерода (II) CО:
СО2+ С = 2СО
С + Н2О (перегретый пар) = СО +Н2
Синтезирован оксид углерода С2О3.
СО2 - кислотный оксид, ему отвечает слабая неустойчивая, существующая только в сильно разбавленных холодных водных растворах угольная кислота Н2СО3. Соли угольной кислоты - карбонаты (см. КАРБОНАТЫ) (К2СО3, СаСО3) и гидрокарбонаты (см. ГИДРОКАРБОНАТЫ) (NaHCO3, Са(НСО3)2).
С водородом (см. ВОДОРОД) графит и древесный уголь реагируют при температуре выше 1200°C, образуя смесь углеводородов. Реагируя со фтором при 900°C, образует смесь фторуглеродных соединений. Пропуская электрический разряд между угольными электродами в атмосфере азота, получают газ циан (CN)2; если в газовой смеси присутствует водород, образуется синильная кислота HCN. При очень высоких температурах графит реагирует с серой, (см. СЕРА) кремнием, бором, образуя карбиды - CS2, SiC, В4С.
Карбиды получают взаимодействием графита с металлами при высоких температурах: карбид натрия Na2C2, карбид кальция CaC2, карбид магния Mg2C3, карбид алюминия Al4C3. Эти карбиды легко разлагаются водой на гидроксид металла и соответствующий углеводород:
Al4C3 + 12Н2О = 4Al(ОН)3 + 3СН4
С переходными металлами углерод образует металлоподобные химически стойкие карбиды, например, карбид железа (цементит) Fe3C, карбид хрома Cr2C3, карбид вольфрама WС. Карбиды - кристаллические вещества, природа химической связи может быть различной.
При нагревании уголь восстанавливает многие металлы из их оксидов:
FeO + C = Fe + CO,
2CuO+ C = 2Cu+ CO2
При нагревании восстанавливает серу(VI) до серы(IV) из концентрированной серной кислотой:
2H2SO4+ C = CO2+ 2SO2+ 2H2O
При 3500°C и нормальном давлении углерод сублимирует.
Применение
Свыше 90% всех первичных источников потребляемой в мире энергии приходится на органическое топливо. 10% добываемого топлива используется в качестве сырья для основного органического и нефтехимического синтеза, для получения пластмасс.
Физиологическое действие
Углерод - важнейший биогенный элемент, является структурной единицей органических соединений, участвующих в построении организмов и обеспечении их жизнедеятельности (биополимеры, витамины, гормоны, медиаторы и другие). Содержание углерода в живых организмах в расчете на сухое вещество составляет 34,5-40% у водных растений и животных, 45,4-46,5% у наземных растений и животных и 54% у бактерий. В процессе жизнедеятельности организмов происходит окислительный распад органических соединений с выделением во внешнюю среду CO2. Углекислый газ (см. УГЛЕРОДА ДИОКСИД) , растворенный в биологических жидкостях и природных водах, участвует в поддержании оптимальной для жизнедеятельности кислотности среды. В составе CaCO3 углерод образует наружный скелет многих беспозвоночных, содержится в кораллах, яичной скорлупе.
При различных производственных процессах частицы угля, сажи, графита, алмаза попадают в атмосферу и находятся в ней в виде аэрозолей. ПДК для углеродной пыли в рабочих помещениях 4,0 мг/м3 , для каменного угля 10 мг/м3.