ж.
Благородный драгоценный металл серебристо-белого цвета, ценимый дороже золота.
ПЛА́ТИНА, платины, мн. нет, жен. (исп. platina, уменьш. к plata - серебро). Драгоценный нержавеющий металл белого цвета, ценимый дороже золота. Самородная платина. Чистая платина. Губчатая платина (см. губчатый).
ПЛА́ТИНА, -ы, жен. Драгоценный тугоплавкий блестящий металл серовато-белого цвета.
| прил. платиновый, -ая, -ое. Платиновая брошь. Платиновая руда. Металлы платиновой группы.
ПЛАТИНА, платина жен. белое золото, самородный (не рудный), ценный металл, тяжелее золота, весьма твердый и огнестойкий. Платинный и платиновый, из нее сделанный, к ней относящийся. Платинистый осмий, иридий, содержащий в себе платину. Платинка жен. бывшая у нас платиновая, трехрублевая монета. Платинчик, платинник муж. платиновый тигель, плавильный горшочек. Платинщик муж. обрабатывающий платину, что требует особого искусства.
ПЛА́ТИНА, -ы, ж
Химический элемент, серовато-белый блестящий с различными оттенками драгоценный металл.
Платина и ее сплавы - материалы электрических контактов, катализаторы при получении азотной и серной кислот. Ювелирные изделия из золота и платины пользуются спросом у всех, кто любит украшения.
ПЛА́ТИНА -ы; ж. [исп. platina] Химический элемент (Pt), благородный металл серебристо-белого цвета, обладающий красивым внешним видом, химической стойкостью и тугоплавкостью (применяется в электро- и радиотехнике, ювелирном деле, как химический катализатор). Самородная п. Кольцо из платины. Сплавы с платиной. П. подорожала.
◁ Пла́тиновый (см.).
* * *
пла́тина (лат. Platinum), химический элемент VIII группы периодической системы, относится к платиновым металлам. Название от испанского platina (уменьшит. от plata - серебро). Плотность 21,45 г/см3, tпл 1769°C. Идёт на изготовление катализаторов (около 50%; частично в виде сплавов с Rh, Pd, Ir), химической аппаратуры; используется в электро- и радиотехнике, ювелирном деле и т. д.
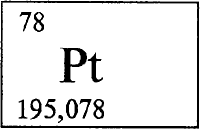
* * *
ПЛАТИНА - ПЛА́ТИНА (лат. Platinum, испанское platina, уменьшительное от plata - серебро), Pt, читается «платина», химический элемент с атомным номером 78, атомная масса 195,083. Платина состоит из четырех стабильных изотопов 194Pt (32,9%), 195Pt (33,8%), 196Pt (25,2%), 198Pt (7,2%) и двух слабо радиоактивных 190Pt (0,013 %, период полураспада Т1/2 = 6,9·1011 лет), 192Pt (0,78 %, Т1/2 = 1015лет). Относится к платиновым металлам (см. ПЛАТИНОВЫЕ МЕТАЛЛЫ) и располагается в 6 периоде, в VIIIB группе периодической системы элементов. Входит в триаду платина, осмий, иридий. Конфигурация двух внешних электронных слоев 5s2p6d96s1. Степени окисления 0, +2, +3, +4, +6 и редко +5 (валентности 0, II, III, IV, V, VI). Наиболее характерна степень окисления +4.
Радиус атома 0,138 нм, ионный радиус иона Pt2+ - 0,074 (координационное число 4), Pt2+ - 0,094 (6) , Pt4+ - 0,0765 (6), Pt5+ - 0.071 нм (6). Энергии ионизации Pt0 - Pt+ - Pt2+ - Pt3+ равны 9,0, 18,56, 23,6 эВ. Электроотрицательность по Полингу 2,2.
История открытия
Платина известна человечеству с древнейших времен. Изделия, содержащие платину, найдены при раскопках древнеегипетских гробниц и древнеиндейских поселений в Колумбии. Первое описание платины в Европе сделал А. де Ульолоа, который участвовал во французской экспедиции в 1736 с целью определения длины экватора. В его записях упоминается благородный металл platina,найденный в колумбийских золотых рудниках.
В 1741 южноамериканские образцы металла были доставлены в Европу, где сначала платину рассматривали как «белое золото». В середине 18 века была установлена элементарная природа платины. В настоящее время «белым золотом» называют сплавы золота и платины. Расплавить чистую платину удалось в 1783 А. Л. Лавуазье (см. ЛАВУАЗЬЕ Антуан Лоран) .
Получение
Производство платины в виде порошка началось в 1805 англичанином У. Х. Волластоном (см. ВОЛЛАСТОН Уильям Хайд) из южноамериканской руды.
В настоящее время платину получают из концентрата платиновых металлов. Концентрат растворяют в царской водке (см. ЦАРСКАЯ ВОДКА), после чего добавляют этанол и сахарный сироп для удаления избытка HNO3. При этом иридий и палладий восстанавливаются до Ir3+ и Pd2+. Последующим добавлением хлорида аммония выделяют (NH4)2PtCl6. Высушенный осадок прокаливают при 800-1000°C:
(NH4)2PtCl6 = N2 + 6HCl + Pt + H2.
Получаемую таким образом губчатую платину подвергают дальнейшей очистке повторным растворением в царской водке, осаждением (NH4)2PtCl6 и прокаливанием остатка. Затем очищенную губчатую платину переплавляют в слитки. При восстановлении платиновых растворов химическим или электрохимическим способом получают мелкодисперсную платину - платиновую чернь.
Нахождение в природе
Платина - один из наиболее редких элементов, ее содержание в земной коре 5·10-7% по массе. Она встречается в природе в сульфидных, медно-никелевых и медно-молибденовых рудах, в виде самородков и самородных сплавов с иридием или палладием. Минералы платины: PtAs2 (сперрилит), PtS (куперит), (Pt,Pd,Ni)S (брэггит).
Физические и химические свойства
Платина - тугоплавкий тяжелый (плотность при 20°C 21,45 г/см3) серебристо-белый металл. Имеет кубическую гранецентрированную решетку, a = 0,392 нм. Температура плавления 1769°C, кипения 4170°C. Проявляет свойства парамагнетика. Металлическая платина хорошо поддается прокату и сварке. В ряду стандартных потенциалов платина расположена правее водорода и с неокисляющими кислотами и водой не реагирует.
По химическим свойствам платина похожа на палладий (см. ПАЛЛАДИЙ (химический элемент)), но проявляет большую химическую устойчивость. Реагирует только с горячей царской водкой:
3Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO + 8H2O
Платина медленно растворяется в горячей серной кислоте и жидком броме. Она не взаимодействует с другими минеральными и органическими кислотами. При нагревании реагирует со щелочами и пероксидом натрия, галогенами (см. ГАЛОГЕНЫ) (особенно в присутствии галогенидов щелочных металлов):
Pt + 2Cl2 + 2NaCl = Na2[PtCl6].
При нагревании платина реагирует с серой, селеном, теллуром, углеродом и кремнием. Как и палладий, платина может растворять молекулярный водород, но объем поглощаемого водорода меньше и способность его отдавать при нагревании у платины меньше.
При нагревании платина реагирует с кислородом с образованием летучих оксидов. Выделены следующие оксиды платины: черный PtO, коричневый PtO2, красновато-коричневый PtO3, а также Pt2O3 и Pt3O4.
Для платины известны гидроксиды Pt(OH)2 и Pt(OH)4. Получают их при щелочном гидролизе соответствующих хлорплатинатов, например:
Na2PtCl4 + 2NaOH = 4NaCl + Pt(OH)2Ї,
Na2PtCl6 + 4NaOH = 6NaCl + Pt(OH)4Ї.
Эти гидроксиды проявляют амфотерные свойства:
Pt(OH)2 + 2NaOH = Na2[Pt(OH)4],
Pt(OH)2 +4HCl = H2[PtCl4] + 2H2O,
Pt(OH)4 + 6HCl = H2[PtCl6] + 4H2O,
Pt(OH)4 + 2NaOH = Na2[Pt(OH)6].
Гексафторид PtF6 - один из сильнейших окислителей, способный окислить молекулы кислорода, ксенона или NO:
O2 + PtF6 = O2+[PtF6]-.
C обнаруженного Н. Бартлеттом (см. БАРТЛЕТТ Нил) взаимодействия между Хе и PtF6, приводящего к образованию XePtF6, началась химия инертных газов. PtF6 получают фторированием платины при 1000 °C под давлением.
Фторирование платины при нормальным давлении и температуре 350-400 °C дает фторид Pt(IV):
Pt + 2F2 = PtF4
Фториды платины гигроскопичны и разлагаются водой.
Тетрахлорид платины (IV) с водой образует гидраты PtCl4·nH2O, где n = 1, 4, 5 и 7. Растворением PtCl4 в соляной кислоте получают платинохлористоводородные кислоты H[PtCl5] и H2[PtCl6].
Синтезированы такие галогениды платины как PtBr4, PtCl2, PtCl2·2PtCl3, PtBr2 и PtI2.
Для платины характерно образование комплексных соединений (см. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ) состава [PtХ4]2- и [PtX6]2-. Изучая комплексы платины, А. Вернер (см. ВЕРНЕР Альфред) сформулировал теорию комплексных соединений и объяснил природу возникновения изомеров в комплексных соединениях.
Применение
Основное применение платина, ее сплавы и соединения находят в автомобилестроении (30-65%), в качестве катализатора для дожигания выхлопных газов автомобилей. 7-12% платины используется в нефтеперерабатывающей промышленности и органическом синтезе (в процессах гидрирования углеводородов), 7-13% - в электротехнике и электронике, 3-17% - в стекольной и керамической промышленности, 2-35% - для изготовления зубных протезов и ювелирных изделий.
Физиологическое действие
Все соединения платины - сильные окислители. И требуют осторожного обращения.
ПЛАТИНА (лат. Platinum) - Pt, химический элемент VIII группы периодической системы, атомный номер 78, атомная масса 195,08, относится к платиновым металлам. Название от исп. platina (уменьшительное от plata - серебро). Плотность 21,45 г/см³, tпл 1769 .С. Платина идет на изготовление катализаторов (ок. 50%; частично в виде сплавов с Rh, Pd, Ir), химической аппаратуры; используется в электро- и радиотехнике, ювелирном деле и т. д.
-ы, ж.
Химический элемент, благородный металл серовато-белого цвета, обладающий большой ковкостью и тягучестью (употребляется в электро- и радиотехнике, ювелирном деле и т. д.).
В толстом кольце из платины горел злым зеленым огнем изумруд. М. Горький, Жизнь Клима Самгина.
[исп. platina]
Pt (platinum),
металлический химический элемент VIIIВ группы периодической системы элементов, наиболее распространенный член семейства платиновых металлов: Ru, Rh, Pd, Os, Ir, Pt. Хотя известны древние предметы искусства, сделанные из Pt, сам металл был обнаружен европейцами лишь в 1557 в Мексике поэтом и путешественником эпохи Возрождения Ю.Скалигером. В 1748 А.де Уллоа описал металл, о котором впервые письменно упомянул Ю.Скалигер. В чистом виде получена в 1803 У.Волластоном, который нашел способ приготовления тонкой платиновой проволоки и ковкой платины для изготовления посуды. Платина встречается в природе в самородном состоянии и в виде соединений. В природных отложениях она бывает в виде песчаноподобных частиц, смешанных с похожими частицами других металлов этой группы или с рудами Cu, Co, Ni и Au. В природе обнаружены и большие самородки платины. Наиболее важными рудами Pt являются сперрилит PtAs2 и куперит PtS. Мировым производителем платины считается Южно-Африканская республика, затем идут Канада и Россия. СВОЙСТВА ПЛАТИНЫ
Атомный номер 78 Атомная масса 195,08 Изотопы
стабильные 190, 192, 194-196, 198
нестабильные 173-189, 191, 193, 197, 199, 200
Температура плавления, ° С 1769 Температура кипения, ° С 3827 Плотность, г/см3 21,45 Твердость (по Моосу) 4,3 Содержание в земной коре, % (масс.) 0,0000005 Степени окисления 0, +2, +4; реже +1, +3, +5, +6
Свойства. Платина - серебристый, сравнительно мягкий, плотный и ковкий металл с высокой прочностью на разрыв. Платина обладает относительно низкой электрической проводимостью и самым низким коэффициентом расширения из всех промышленных металлов. Она не тускнеет на воздухе, заметно испаряется при температуре красного каления. Галогены (и в том числе фтор) не взаимодействуют с Pt при обычной температуре, и это единственный металл, нерастворимый в любой из минеральных кислот. Но смесь концентрированных соляной и азотной кислот ("царская водка") и смесь соляной и хлорной кислот растворяют платину. При высокой температуре платина реагирует с расплавленными нитратами, с кислыми сульфатами, гидроксидами, пероксидами, сульфидами, I2, P, As, C, Si, Se и Te.
Основные соединения. При нагревании с царской водкой платина образует тетрахлороплатинат водорода H2PtCl4, а в избытке HCl - соответственно H2PtCl6 - гексахлороплатинат водорода. Гексахлороплатинат натрия Na2PtCl6 хорошо растворим в воде и даже в 75%-ном растворе спирта, чем отличается от соответствующих солей калия и аммония, и поэтому может быть отделен от них по обычной методике качественного анализа. При добавлении аммиака к солям платины получают комплексные соединения - аммины Pt(NH3)4Cl2 и Pt(NH3)6Cl4. Известны также флуоресцирующие двойные соли типа Pt(CN)2ЧBa(CN)2Ч4H2O. При нагревании H2PtCl4 с хлором образуется PtCl4, который при 370° С диссоциирует на PtCl2 + Cl2. Дихлорид PtCl2 в свою очередь разлагается при 200° С до губчатой платины. Такая платина при температуре красного каления способна адсорбировать большие объемы водорода, сохраняя адсорбционные свойства и при комнатной температуре. Платиновая чернь представляет собой более дисперсную форму платины.
См. также ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ.
Применение. Важнейшее применение платина находит как катализатор нейтрализации выхлопных газов и для увеличения октанового числа бензинов. Благодаря относительной инертности платина в свободном состоянии и в сплавах с Rh почти незаменима в компьютерной и электронной технике, магнитных контактах, свечах зажигания. Платина и ее сплавы играют важную роль в химической технологии, например в каталитическом производстве азотной кислоты из аммиака, в фильерах при изготовлении стекловолокна, в качестве электродов анодного окисления (перхлораты, пероксиды) или электроосаждения (Ni, Rh), для изготовления устойчивых к коррозии и термостойких деталей измерительной и регистрирующей аппаратуры. Платина широко используется в производстве ювелирных изделий, стоматологических сплавов, медицинского и хирургического инструмента.
ЛИТЕРАТУРА
Ливингстон С. Химия рутения, родия, палладия, осмия, иридия, платины. М., 1978 Платина, ее сплавы и композиционные материалы. М., 1980
ПЛАТИН|А (1*), Ы с. Кусок ткани, часть одежды (?):
ст҃ии пр҃рци. ап(с)ли ст҃ли и прп҃бнии. ликь мч҃нчскыи… сице и чю(д)съ дѣтели спо(д)биша(с) быти. ли в рака(х) лежаще мюро источаю(т) ли костию ли власо(м). или планитою [в др. сп. платиною] ризъ своихъ бѣсы изгонѧть. Пал 1406, 20а.
пла́тина, пла́тины, пла́тин, пла́тине, пла́тинам, пла́тину, пла́тиной, пла́тиною, пла́тинами, пла́тинах
платина I
химический элемент с атомным номером 78, обозначается химическим символом Pt, относящийся к группе благородных металлов
Один из природных изотопов платины радиоактивен.
простое вещество, состоящее из атомов платины , при нормальных условиях тяжёлый светло-серый металл
Платину в больших количествах добывали в Южной Америке и на Урале.
платина II
основание часового механизма, на котором монтируются все его детали
Это слово было заимствовано из французского, где существительное platine является уменьшительным к plata - "серебро".
Из фр. яз. в XIX в. (вначале было ударение на и: платина). Фр. platine < исп. platina, от plata - «серебро».
Заимств. в XIX в. из франц. яз., где platine < исп. platina, суф. уменьшит.-ласкат. производного от plata «серебро».
пла́тина
Через нем. Platina или прямо из исп. platina - то же, производного от исп. рlаtа "серебро" (Преобр. II, 69; Клюге-Гётце 449).
ПЛАТИНА ы, ж. platine f. текст. Металлическая пластинка; плоская часть разных инструментов; зажим, крючок, проступной крючок. Сл. 1948. Платины - тонкие стальные пластинки фигурной формы, расположенные между иглами. Они предназначены для изгибания нити в петлю, сбрасывания и оттягивания готовых петель <вязальных машин >. 1975. Шишкин Трикотаж 27. Носик платины. Сл. 1948. Платинный ая, ое. Платинная петля. Текст. сл. 62.
ПЛАТИНА (исп., от plata - серебро). Самый тяжелый из благородных металлов; с виду похож на серебро, встречается в перуанских, бразильских и уральских россыпях.
- Драгоценный металл.
- Металл, из которого делался орден Суворова I степени.
- Химический элемент, Pt.
- Химики XVIII века называли её «гнилое золото» и «лягушачье золото».
- Материал, из которого должен быть сделан подарок, преподнесённый к семидесятой годовщине свадьбы.
Пла́тина саморо́дная - группа минералов, твёрдых растворов в платине других металлов, преимущественно Fe. Разновидности: ферроплатина (20-50% Fe), иридистая Pt (10,4-37,5% Ir), палладистая Pt (14-40% Pd) и др. Стально-серые вкрапленности в породе, зёрна в россыпях. Твёрдость 3,5-5,5; плотность 13,1-21,5 г/см3; ковкая. Месторождения в ультраосновных породах (коренные) и россыпи.
* * *
ПЛАТИНА САМОРОДНАЯ - ПЛА́ТИНА САМОРО́ДНАЯ, группа минералов, твердых растворов в платине других металлов, преимущественно Fe. Разновидности: ферроплатина (20-50% Fe), иридистая Pt (10,4-37,5% Ir), палладистая Pt (14-40% Pd) и др. Стально-серые вкрапленности в породе, зерна в россыпях. Твердость 3,5-5,5; плотность 13,1-21,5 г/см3; ковкий. Месторождения в ультраосновных (см. УЛЬТРАОСНОВНЫЕ ГОРНЫЕ ПОРОДЫ) породах (коренные) и россыпи (см. РОССЫПНЫЕ МЕСТОРОЖДЕНИЯ) .
ПЛАТИНА САМОРОДНАЯ - группа минералов, твердых растворов в платине других металлов, преимущественно Fe. Разновидности: ферроплатина (20-50% Fe), иридистая Pt (10,4-37,5% Ir), палладистая Pt (14-40% Pd) и др. Стально-серые вкрапленности в породе, зерна в россыпях. Твердость 3,5-5,5; плотность 13,1-21,5 г/см³ ковкий. Месторождения в ультраосновных породах (коренные) и россыпи.
платина́т, платина́ты, платина́та, платина́тов, платина́ту, платина́там, платина́том, платина́тами, платина́те, платина́тах