МОСАНДЕР (Mosander) Карл Густав (1797-1858) - шведский химик. Открыл редкоземельные элементы лантан (1839), тербий и эрбий (1843).
мосандер карл густав
Энциклопедический словарь
Мо́сандер Карл Густав (Mosander) (1797-1858), шведский химик. Открыл редкоземельные элементы лантан (1839), тербий и эрбий (1843).
* * *
МОСАНДЕР Карл Густав - МО́САНДЕР (Mosander) Карл Густав (1797-1858), шведский химик. Открыл редкоземельные элементы лантан (1839), тербий и эрбий (1843).
Полезные сервисы
празеодим
Энциклопедический словарь
Празеоди́м (лат. Praseodymium), химический элемент III группы периодической системы; относится к лантаноидам. Металл, плотность 6,475 г/см3, tпл 932°C. Легирующая добавка к стали, сплавам цветных металлов, магнитным сплавам.
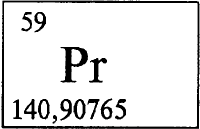
* * *
ПРАЗЕОДИМ - ПРАЗЕОДИ́М (лат. Praseodimium), Pr (читается «празеодим»), химический элемент с атомным номером 59, атомная масса 140,9077. В природе один стабильный нуклид 141Pr. Конфигурация трех внешних электронных слоев 4s2p6d10f35s2p65d06s2. Образует соединения в степенях окисления +2, +3 и +4 (валентности II, III и IV).
Относится к редкоземельным элементам цериевой подгруппы лантаноидов. Расположен в группе IIIB, 6 периода периодической системы.
Радиус нейтрального атома Pr 0,182 нм, радиус иона Pr3+ - 0,113 (координационное число 6) иона Pr 4+- 0,099 нм (координационное число 6). Энергии последовательной ионизации атома Pr 5,42, 10,55, 21,63, 38,96 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,07.
История открытия
Празеодим был открыт в 1885 австрийским химиком К. Ауэром фон Вельсбахом (см. АУЭР фон ВЕЛЬСБАХ Карл). Он установил, что обнаруженный в 1839 шведским химиком К. Г. Мосандером (см. МОСАНДЕР Карл Густав) элемент дидим является смесью двух элементов с близкими физическими и химическими свойствами, которые он дал название неодим (см. НЕОДИМ) и празеодим (от греч. «празеос» - светло-зеленый и «дидимос» - двойник).
Нахождение в природе
Содержание в земной коре 7·10-4% по массе. Входит в состав таких минералов, как бастнезит (см. БАСТНЕЗИТ), монацит, (см. МОНАЦИТ) лопарит (см. ЛОПАРИТ) ,самарските и апатите (см. АПАТИТЫ) .
Получение
При выделении из природных объектов Pr концентрируется вместе с легкими лантаноидами, дальнейшее разделение проводят методами ионной хроматографии (см. ХРОМАТОГРАФИЯ) или экстракции (см. ЭКСТРАКЦИЯ ЖИДКОСТНАЯ). На последней стадии отделяют Pr от неодима. Металлический Pr получают электролизом (см. ЭЛЕКТРОЛИЗ) расплава хлорида празеодима PrCl3.
Физические и химические свойства
Празеодим - светло-серый металл. До 796°C существует a-модификация с гексагональной решеткой типа лантана, параметры а = 0,36725 нм и с = 1,18354 нм, от 796°C до температуры плавления (932°C) - b-модификация с кубической решеткой типа a-Fe. При высоких давлениях существует кубическая модификация празеодима. Температура кипения 3512°C, плотность a-Pr 6,475 кг/дм3.
На воздухе празеодим медленно окисляется, при нагревании возгорается, образуя оксид Pr6O11. Прокаливая этот оксид в атмоcфере H или CH4, образуется оксид Pr2O3. Если окисление празеодима проводить в атмосфере O2 при давлении 10 МПа, образуется диоксид празеодима PrO2. Оксиды Pr имеют основный характер; при реакциях этих оксидов с минеральными кислотами возникают соответствующие соли Pr3+.
При нагревании Pr реагирует с галогенами, (см. ГАЛОГЕНЫ) образуя тригалогениды, такие как PrCl3 и PrF3.
Применение
Празеодим - компонент миш-металла (см. МИШ-МЕТАЛЛ), легких сплавов с магнием (см. МАГНИЙ) и алюминием (см. АЛЮМИНИЙ), легирующая добавка к стали и другим сплавам. Оксиды празеодима - компоненты стекол для защиты глаз от желтого излучения Na, а также УФ и ИК излучения при сварке, обесцвечивают железосодержащие стекла, пигменты для цветного стекла, художественной керамики. Смесь оксидов Pr(III) и Ce(IV) - основа полирующих порошков для оптики, компоненты катализаторов крекинга.
Полезные сервисы
эрбий
Энциклопедический словарь
Э́рбий (лат. Erbium), химический элемент III группы периодической системы, относится к лантаноидам. О названии см. Иттрий. Металл, плотность 9,062 г/см3, tпл 1522°C. Компонент магнитных сплавов с железом, кобальтом, никелем.
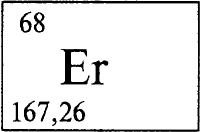
* * *
ЭРБИЙ - Э́РБИЙ (лат. Erbium), Er (читается «эрбий»), химический элемент с атомным номером 68, атомная масса 167,26. Является смесью шести стабильных нуклидов: 162Er (содержание в природной смеси 0,14% по массе), 164Er (1,61%), 166Er (33,6%), 167Er (22,95%), 168Er (26,8%) и 170Er (14,9%). Конфигурация трех внешних электронных слоев 4s2p6d10f125s2p66s 2. Образует соединения в степенях окисления +3 (валентность III) и, редко, +1 (валентность I). Лантаноид (см. ЛАНТАНОИДЫ). Расположен в группе IIIB в 6 периоде периодической системы.
Радиус нейтрального атома Er 0,175 нм, радиус иона Er 3+- 0,103 нм (координационное число 6) и 0,120 нм (координационное число 9). Энергии последовательной ионизации атома 6,10, 11,93, 22,74, 42,65 и 65,1 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,11.
История открытия
Впервые эрбий был выделен в 1843 шведским химиком К. Г. Мосандером (см. МОСАНДЕР Карл Густав) из минерала иттербита, найденного около селения Иттербю. Последующие исследования показали, что в выделенной из минерала «эрбиевой земле», кроме эрбия, содержались также тулий, гольмий (см. ГОЛЬМИЙ) и диспрозий (см. ДИСПРОЗИЙ) .
Нахождение в природе
Содержание Er в земной коре 3,3·10-3%. Входит в состав таких минералов, как ксенотим (см. КСЕНОТИМ), бастнезит (см. БАСТНЕЗИТ), монацит (см. МОНАЦИТ), эвксенит, лопарит. (см. ЛОПАРИТ)
Получение
При выделении концентрируется с тяжелыми лантаноидами. Дальнейшее разделение проводят методами ионной хроматографии (см. ХРОМАТОГРАФИЯ) или экстракции (см. ЭКСТРАКЦИЯ ЖИДКОСТНАЯ). Металлический эрбий получают электролизом расплава хлорида (фторида) эрбия ErCl3 (ErF3).
Физические и химические свойства
Эрбий - белый металл. Гексагональная решетка с параметрами а = 0,35588 нм и с = 0,55874 нм. Температура плавления 1522°C, температура кипения 2510°C, плотность 9,062 кг/дм3.
Устойчив на воздухе. При нагревании реагирует с кислородом (см. КИСЛОРОД), галогенами (см. ГАЛОГЕНЫ) и другими неметаллами. Оксид эрбия Er2O3 получают прокаливанием нитрата, сульфата, оксалата и других солей эрбия при температуре 800-1000°C. Обладает основными свойствами, ему отвечает основание Er(ОН)3 средней силы.
Эрбий взаимодействует с минеральными кислотами, образуя соли эрбия(III). Ионы Er3+ окрашивают раствор в розовый цвет. К растворимым в воде солям эрбия относятся хлорид, нитрат, ацетат и сульфат, плохо растворимым - оксалат, фторид, карбонат и фосфат.
При взаимодействии Er с тригалогенидами эрбия образуются соединения ErHal с кластерами Er7Hal10, Er6Hal7 и другими.
Применение
Применяют как активатор люминофоров, для изготовления магнитных материалов.
Иллюстрированный энциклопедический словарь
ЭРБИЙ (Erbium), Er, химический элемент III группы периодической системы, атомный номер 68, атомная масса 167,26; относится к редкоземельным элементам; металл. Открыт шведским химиком К. Мосандером в 1843.