Неоди́м (лат. Neodymium), химический элемент III группы периодической системы, относится к лантаноидам. Название от греческого néos - новый и dídymos - близнец (празеодима) связано с историей открытия. Металл; плотность 6,908 г/см3, tпл 1016°C. Компонент сплавов (например, с Mg, Al или Ti) для самолёто- и ракетостроения, лазерных материалов.
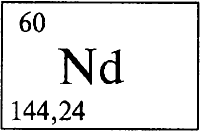
* * *
НЕОДИМ - НЕОДИ́М (лат. Neodimium), Nd (читается «неодим»), химический элемент с атомным номером 60, атомная масса 144,24. Состоит из пяти изотопов 142Nd (27,07%), 143Nd (12,17%), 145Nd (8,30%), 146Nd (17,22%) и 148Nd (5,78%) и радиоактивных изотопов 144Nd (23,78%, период полураспада Т1/2 = 5.1015 лет) и 150Nd (5,67%, период полураспада Т1/2 = 2.1015 лет). Конфигурация внешних электронных слоев 4s2p6d10f4 5s2p66s2. Степени окисления в соединениях +3 (валентность III), реже +4 и +2 (валентности IV и II).
Относится к редкоземелььным элементам (цериевая подгруппа лантаноидов). Расположен в группе III B в 6 периоде периодической системы.
Радиус нейтрального атома 0,182 нм, радиус иона Lu3+ - 0,112-0,141 нм, иона Nd2+- 0,143- 0,149 нм. Энергии ионизации 5,49, 10,72, 22,1, 40,41 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,07.
История открытия
Неодим открыл в 1885 австрийский химик К. Ауэр фон Вельсбах (см. АУЭР фон ВЕЛЬСБАХ Карл), который установил, что обнаруженный в 1839 году французским химиком К. Г. Мосандером (см. МОСАНДЕР Карл Густав) элемент дидим на самом деле представляет смесь двух элементов с близкими физическими и химическими свойствами, которым он дал названия неодим и празеодим (см. ПРАЗЕОДИМ). История открытия неодима отражена в его названии (от греч. neos - новый и didymos - двойник).
Нахождение в природе
Неодим - один из наиболее распространенных редкоземелььных элементов. Содержание его в земной коре 2,5·10-3%, в морской воде 9,2·10-6мг/л. Входит в состав минералов бастнезит (см. БАСТНЕЗИТ), монацит (см. МОНАЦИТ) и лопарит (см. ЛОПАРИТ).
Получение
При разделении редкоземелььных элементов неодим концентрируется вместе с легкими лантаноидами и выделяется вместе с празеодимом. Дальнейшее разделение проводят методами ионной хроматографии или экстракции. Металлический неодим получают электролизом расплава хлорида или фторида неодима NdF3, NdCl3.
Физические и химические свойства
Неодим - светло-серый металл. Ниже 885°C устойчива a-модификация с гексагональной решеткой типа лантана, а = 0,36579 нм и с = 1,17002 нм, выше 885°C и до температуры плавления 1016°C - b-модификация с кубической решеткой типа a-Fe. Температура кипения 3027°C, плотность a-Nd 6,908 кг/дм3.
К окислению неодим менее устойчив, чем тяжелые лантаноиды. При нагревании на воздухе быстро окисляется, образуя оксид Nd2O3. Бурно реагирует с кипящей водой с выделением водорода и образованием гидроксида Nd(OH)3:
2Nd + 6Н2O = 3Nd(OH)3 + 3Н2
При нагревании реагирует с галогенами, азотом, водородом, серой и другими неметаллами. Бурно реагирует с минеральными кислотами.
Оксид Nd2О3 обладает основными свойствами, ему отвечает основание Nd(ОН)3 средней силы. К растворимым в воде солям неодима относятся хлорид, нитрат, ацетат и сульфат, к плохо растворимым - оксалат, фторид, карбонат и фосфат.
Применение
Неодим - компонент мишметалла, легких сплавов с магнием (см. МАГНИЙ) и алюминием. (см. АЛЮМИНИЙ) Сплав неодима, железа (см. ЖЕЛЕЗО) и бора (см. БОР (химический элемент)) применяют для изготовления постоянных магнитов. Оксид и фосфат неодима - пигмент при варке цветного стекла, керамики. Оксид неодима Nd2О3 используют при варке неодимового стекла (лазерный материал), служит добавкой при получении иттрий-алюминиевых гранатов.