м.
Химический элемент, мягкий металл серебристо-белого цвета, сходный по своим свойствам с калием и натрием.
м.
Химический элемент, мягкий металл серебристо-белого цвета, сходный по своим свойствам с калием и натрием.
РУБИ́ДИЙ, рубидия, муж. (от лат. rubidus - красноватый). Химический элемент - мягкий металл серебристо-белого цвета, по свойствам сходный с калием и натрием.
РУБИ́ДИЙ, -я, м
Химический элемент, серебристо-белый легкоплавкий металл (один из самых активных щелочных металлов).
В соприкосновении с воздухом рубидий воспламеняется, образуя главным образом различные перекиси.
РУБИ́ДИЙ -я; м. [от лат. rubidus - красноватый] Химический элемент (Rb), мягкий металл серебристо-белого цвета, по своим свойствам сходный с калием и натрием.
◁ Руби́диевый, -ая, -ое.
* * *
руби́дий (лат. Rubidium), химический элемент I группы периодической системы; относится к щелочным металлам. Название от лат. rubidus - тёмно-красный (открыт по линиям в красной части спектра). Серебристо-белый металл пастообразной консистенции. Плотность 1,532 г/см3, tпл 39,32°C, tкип 687°C. На воздухе мгновенно воспламеняется, с водой реагирует со взрывом. В природе рассеян, сопутствует калию и литию и добывается из их минералов. Применяется ограниченно (катоды для фотоэлементов, добавка в газоразрядные трубки, катализатор в органическом синтезе).
* * *
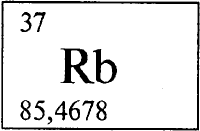
РУБИДИЙ - РУБИ́ДИЙ (лат. rubidium, от лат. rubidus - красный), Rb (читается «рубидий»), химический элемент с атомным номером 37, атомная масса 85,4678. Природный рубидий состоит из смеси стабильного нуклида 85Rb (72,15% по массе) и слабо --радиоактивного 87Rb (период полураспада Т1/2 = 4,8·1010 лет). Расположен в группе IA (щелочные металлы), в 5-м периоде. Электронная конфигурация внешнего слоя 5s1, Степень окисления +1 (валентность I).
Радиус нейтрального атома рубидия 0,248 нм, радиус иона Rb+0,166 нм (координационное число 6). Энергии последовательной ионизации атома Rb 4,177, 27,5, 40,0, 52,6 и 71 эВ. Сродство к электрону 0,49 эВ. Работа выхода электрона 2,16 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 0,8.
История открытия
Немецкие исследователи Р. В. Бунзен (см. БУНЗЕН Роберт Вильгельм) и Г. Р. Кирхгоф выполнили в 1861 спектральные исследования минерала лепидолита (см. ЛЕПИДОЛИТ) и осадка, образующегося после выпаривания минеральных вод из источников Шварцвальда. Спектры содержали темно-красную линию, принадлежащую новому элементу.
После выпаривания минеральных вод из полученного остатка с помощью хлорплатината аммония (NH4)2PtCl6 была осаждена смесь хлорплатинатов калия, рубидия и цезия. Затем, хлорплатинаты были переведены в карбонаты и в соли винной кислоты - тартраты. Путем многократной дробной перекристаллизации кислых тартратов Бунзену удалось очистить рубидий от калия и цезия и получить первый препарат соли рубидия. В 1863 Бунзен за счет восстановления кислого тартрата рубидия с помощью сажи приготовил первый образец металлического рубидия.
Нахождение в природе
Содержание рубидия в земной коре 1,5·10 -2% по массе. Не образует собственных минералов, как правило, сопутствует K или Li. Находится в минеральных источниках, озерной, морской и подземной водах.
Получение
Рубидий в основном получают при переработке или лепидолита на соединения Li, или карналлита, служащего сырьем при производстве Mg. Остаток, образующийся после отделения основных количеств Li, K и Mg и содержащий соли K, Rb и Cs, разделяют на фракции методами дробной кристаллизации, сорбции, экстракции и ионного обмена.
Металлический рубидий обычно готовят восстановлением галогенидов Rb кальцием (см. КАЛЬЦИЙ) или магнием. (см. МАГНИЙ)
Физические и химические свойства
Рубидий - мягкий серебристо-белый металл.
При обычной температуре имеет пастообразную консистенцию, температура плавления +39,32°C. Температура кипения рубидия 687,2°C. Кристаллическая решетка металла кубическая объемно центрированная, параметр ячейки а = 0,570 нм. Рубидий - легкий металл, его плотность 1,532 кг/дм3.
Реакционная способность рубидия очень высока. Его стандартный электродный потенциал -2,925 В. На воздухе и в атмосфере кислорода металлический рубидий воспламеняется, образуя смесь пероксида рубидия Rb2O2 и надпероксид рубидия RbO2. При незначительном содержании кислорода в газе, с которым реагирует Rb, возможно образование и оксида Rb2O. C водой рубидий реагирует со взрывом:
2Rb + 2H2O = 2RbOH + H2
При нагревании под повышенным давлением Rb реагирует с H с образованием гидрида RbH. Rb непосредственно реагирует с галогенами, S с образованием сульфида Rb2S. С азотом рубидий в обычных условиях не реагирует, а нитрид рубидия Rb3N образуется при пропускании электрического разряда между электродами из рубидия, помещенными в жидкий азот. При нагревании рубидий реагирует с красным фосфором, образуя фосфид рубидия Rb2P5. Также при нагревании рубидий реагирует с графитом, причем в зависимости от условий проведения реакции возникают карбиды составов C8Rb и C24Rb.
Для рубидия характерно взаимодействие с аммиаком с образованием амида RbNH2. При реакции рубидия с ацетиленом возникает ацетиленид Rb2C2. Металлический рубидий способен восстанавливать кремний из стекла и из SiO2.
Со многими металлами рубидий образует интерметаллиды.
Гидроксид рубидия RbOH - сильное хорошо растворимое в воде основание, ведет себя аналогично КОН и NaOH.
Такие соли рубидия, как хлорид RbCl, сульфат Rb2SO4, нитрат RbNO3, карбонат Rb2CO3 хорошо растворимы в воде перхлорат рубидия RbClO4 и хлорплатинат рубидия Rb2PtCl6 плохо растворимы в воде
Применение
Металлический рубидий входит в состав смазочных композиций, используемых в реактивной и космической технике. Используется как компонент материала катодов фотоэлементов и фотоэлектрических умножителей. Пары рубидия используются в разрядных трубках, в лампах низкого давления. Некоторые соединения рубидия используют при изготовлении специальных стекол.
Особенности обращения
Хранят в ампулах из стекла пирекс в атмосфере аргона или в стальных герметичных сосудах под слоем обезвоженного вазелинового масла или парафина.
РУБИДИЙ (лат. Rubidium) - Rb, химический элемент I группы периодической системы Менделеева, атомный номер 37, атомная масса 85,4678. Относится к щелочным металлам. Название от лат. rubidus - темно-красный (открыт по линиям в красной части спектра). Серебристо-белый металл пастообразной консистенции. Плотность 1,5248 г/см³, tпл39,5 .С, tкип 685 .С. На воздухе мгновенно воспламеняется, с водой реагирует со взрывом. В природе рассеян, сопутствует калию и литию и добывается из их минералов. Применяется ограниченно (катоды для фотоэлементов, добавка в газоразрядные трубки, катализатор в органическом синтезе).
-я, м.
Химический элемент, мягкий металл серебристо-белого цвета, по своим свойствам сходный с калием и натрием.
[От лат. rubidus - красноватый]
РУБИДИЙ (Rubidium), Rb, химический элемент I группы периодической системы, атомный номер 37, атомная масса 85,4678; относится к щелочным металлам. Открыт немецкими учеными Р. Бунзеном и Г. Кирхгофом в 1861.
- Щелочной металл.
- «Красный» среди химических элементов.
- Химический элемент, Rb.
- Металл, о котором твердил попугай-контрамот из романа братьев Стругацких «Понедельник начинается в субботу».