м.
Химический элемент, относящийся к лантаноидам, редкий металл серебристо-белого цвета, встречающийся в природе в соединениях.
м.
Химический элемент, относящийся к лантаноидам, редкий металл серебристо-белого цвета, встречающийся в природе в соединениях.
ГО́ЛЬМИЙ -я; м. [лат. Holmium] Химический элемент (Но), серебристо-белый металл, относящийся к лантаноидам (используется при производстве специальных стёкол и т.п.).
* * *
Го́льмий (лат. Holmium), химический элемент III группы периодической системы, относится к лантаноидам. Название от латинского Holmia - Стокгольм. Серебристо-белый металл; плотность 8,80 г/см3, tпл 1470ºC. Компонент специальных стёкол, активатор люминофоров.
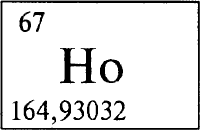
* * *
ГОЛЬМИЙ - ГО́ЛЬМИЙ (лат. Holmium, от латинского Holmia - Стокгольм), Но (читается «гольмий»), химический элемент с атомным номером 67, атомная масса 164,9304. В природе один стабильный изотоп165Ho. Конфигурация трех внешних электронных слоев 4s2p6d10f115s2p66s2. Степени окисления в соединениях +3 (валентность III), реже +2 (валентность II).
Относится к редкоземельным элементам (иттриевая подгруппа лантаноидов). Расположен в III B группе, в 6 периоде периодической системы. Радиус нейтрального атома 0,176 нм, радиус иона Но3+- 0,104-0,121 нм. Энергии ионизации 6,02, 11,80, 22,84, 42,48 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1,1.
История открытия
Открыт в 1879 шведским химиком П. Клеве (см. КЛЕВЕ Пьер Теодор). Исследуя выделенный незадолго до этого К. Мосандером (см. МОСАНДЕР Карл Густав) оксид эрбия (см. ЭРБИЙ) («эрбиевую землю»), он обнаружил смесь трех элементов - эрбия, гольмия и тулия (см. ТУЛИЙ).
Нахождение в природе
Содержание в земной коре 1,310-4% по массе, в морской воде 2,210-7 мг/л. Вместе с другими редкоземельными элементами находится в минералах монаците (см. МОНАЦИТ), апатите (см. АПАТИТ), бастензите (см. БАСТНЕЗИТ) и других.
Получение
Гольмий получают восстановлением фторида гольмия HoF3 кальцием.
Физические и химические свойства
Гольмий - серебристо-серый металл.
Ниже 1428 °C устойчив a-Но с гексагональной решеткой, а = 0,35773 нм, с = 0,56158 нм, выше 1428 °C - b-Но с кубической решеткой. Температура плавления 1470 °C, температура кипения 2700 °C, плотность 8,799 кг/дм3.
На воздухе гольмий медленно окисляется, быстро - при температуре выше 100 °C. При нагревании реагирует с галогенами (см. ГАЛОГЕНЫ), азотом (см. АЗОТ), водородом (см. ВОДОРОД).
Оксид Но2О3 (светло-желтые кристаллы) обладает основными свойствами, ему отвечает основание Но(ОН)3.
Применение
Является компонентом магнитных сплавов, соединения используются как компоненты специальных стекол, как активатор люминофоров и материалов микроэлектроники.
ГОЛЬМИЙ (лат. Holmium) - Но, химический элемент III группы периодической системы, атомный номер 67, атомная масса 164,9304, относится к лантаноидам. Название от латинского Holmia - Стокгольм. Серебристо-белый металл; плотность 8,80 г/см³, tпл 1470 .С. Компонент специальных стекол, активатор люминофоров.
ГОЛЬМИЙ (Holmium), Ho, химический элемент III группы периодической системы, атомный номер 67, атомная масса 164,9304; относится к редкоземельным элементам; металл. Открыт шведским химиком П. Клеве в 1879.
го́льмий
(назв. в честь родины ученого, открывшего элемент лат. holmia Стокгольм) хим. элемент из сем.. лантаноидов, символ Ho (лам. holmium), металл.
- Редкоземельный металл.
- Химический элемент, Ho.
- Этот химический элемент получил своё название в честь латинского названия города Стокгольм.