Авога́дро, нескл., муж.: зако́н Авога́дро, постоя́нная (число́) Авога́дро
авогадро (avogadro) амедео
Большой энциклопедический словарь
АВОГАДРО (Avogadro) Амедео (1776-1856) - итальянский физик и химик. В 1811 выдвинул молекулярную гипотезу строения вещества, установил один из газовых законов, названный его именем.
Полезные сервисы
авогадро амедео
Энциклопедический словарь
Авога́дро Амедео (Avogadro) (1776-1856), итальянский физик и химик. В 1811 выдвинул молекулярную гипотезу строения вещества, установил один из газовых законов, названный его именем.
* * *
АВОГАДРО Амедео - АВОГА́ДРО (Avogadro) Амедео (9 августа 1776, Турин - 9 июля 1856), итальянский физик и химик, член Туринской АН (1819).
Получил юридическое образование в Туринском университете (1792). В 1800 начал самостоятельно изучать физику и математику. С 1806 работал демонстратором в колледже при Туринской академии. С 1809 - профессор в колледже Верчелли, в 1820-1822 и 1834-1850 заведовал кафедрой математической физики в Туринском университете.
Основные работы посвящены молекулярной физике. В 1811 выдвинул молекулярную гипотезу строения вещества, установил один из газовых законов, названный его именем. Согласно этому закону в одинаковых объемах газов при одинаковых значениях температуры и давления содержится одинаковое количество молекул. Исходя из этого, разработал метод определения молекулярного и атомного весов. Именем Авогадро названа универсальная постоянная - число молекул в одном моле идеального газа (число Авогадро). Установил количественный атомный состав молекул некоторых веществ, для которых он ранее был определен неправильно (вода, водород, кислород, азот, оксиды азота, хлора и др.). Первым обратил внимание на аналогию в свойствах азота, фосфора. мышьяка и сурьмы. Эти химические элементы впоследствии составили главную подгруппу пятой группы периодической системы. В 20-40-х гг. 19 в. занимался электрохимией, изучал тепловое расширение тел, теплоемкости. Автор четырехтомного труда «Физика весовых тел, или трактат об общей конституции тел» (1837-1841), который стал первым руководством по молекулярной физике.
Энциклопедия Кольера
АВОГАДРО Амедео (Avogadro, Amedeo)
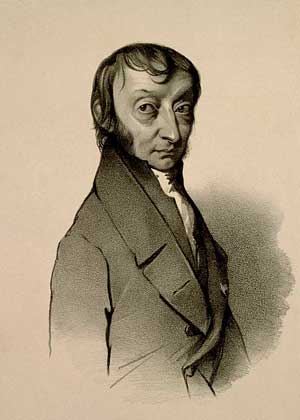
АМЕДЕО АВОГАДРО
(1776-1856), итальянский физик и химик. Родился 9 августа 1776 в Турине в семье чиновника судебного ведомства. Получил юридическое образование и в 1796 стал доктором права. Уже в юности заинтересовался естественными науками, изучал в свободное время физику и математику. С 1806 - демонстратор в колледже при Туринской академии, с 1809 - преподаватель физики Королевского лицея в Верчелли близ Турина, в 1820-1822 и 1834-1850 - профессор физики Туринского университета. В 1811 Авогадро выдвинул гипотезу, что молекулы простых газов состоят из одного или нескольких атомов, и на этом основании сформулировал закон, согласно которому равные объемы всех газов при одинаковой температуре и давлении содержат одинаковое число молекул (число Авогадро). Гипотеза Авогадро была окончательно принята химиками спустя почти полвека. Основной причиной невнимания к идеям Авогадро было то, что большинство его современников не понимали различия между простыми и сложными молекулами (атомами и молекулами в современной терминологии). Против Авогадро выступили многие ведущие ученые того времени, в том числе Дж.Дальтон, У.Волластон, Й.Берцелиус, причем Дальтон утверждал: "Никому не дано разделить атом". Признанию гипотезы Авогадро содействовало выступление его соотечественника С.Канниццаро на Международном конгрессе химиков в Карлсруэ в 1860, который ярко и убедительно изложил закон Авогадро. Неоценимое значение закона Авогадро состояло в том, что он четко разграничивал молекулы и атомы, и это способствовало точному определению атомных и молекулярных масс и формулированию такого понятия, как структура молекул. В.Нернст назвал закон Авогадро "рогом изобилия, дарованным нам молекулярной теорией". Именем Авогадро названа универсальная постоянная (число Авогадро) - число молекул в 1 моле идеального газа. Умер Авогадро в Турине 9 июля 1856.
ЛИТЕРАТУРА
Быков Г.В. Амедео Авогадро. М., 1970
Полезные сервисы
авогадро закон
Энциклопедический словарь
Авога́дро зако́н - в равных объёмах идеальных газов при одинаковых давлении и темп-ре содержится одинаковое число молекул; открыт закон Авогадро в 1811.
* * *
АВОГАДРО ЗАКОН - АВОГА́ДРО ЗАКО́Н, один из основных законов идеальных газов (см. ИДЕАЛЬНЫЙ ГАЗ): в равных объемах идеальных газов при одинаковых давлении и температуре содержится одинаковое число молекул. Число молекул в одном моле называют постоянной Авогадро (см. АВОГАДРО ПОСТОЯННАЯ) или числом Авогадро. Закон был открыт А. Авогадро (см. АВОГАДРО Амедео) в 1811.
Согласно закону Авогадро, 1 моль (см. МОЛЬ) любого идеального газа при нормальных условиях занимает одинаковый объем. При давлении р =101,325 кПа и температуре Т = 273,15 К этот объем равен 22,41383 м3. Следовательно, моль любого вещества содержит одно и то же число молекул, равное числу Авогадро 6,022045(31).1023 моль-1.
Из закона Авогадро следует, что при одних и тех же давлении и температуре плотности двух идеальных газов прямо пропорциональны, а удельные объемы обратно пропорциональны их молекулярным массам.
На основе закона Авогадро в дальнейшем стало развиваться атомно-молекулярное учение, которое является следствием кинетической теории газов (см. КИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗОВ). Закон Авогадро широко применяется в химии только с 1860 г., но имел громадное значение для ее развития, так как давал возможность определять вес тел, способных переходить в газообразное или парообразное состояние. Я. Вант-Гофф (см. ВАНТ-ГОФФ Якоб Хендрик), один из основоположников физической химии, распространил законы идеальных газов на разбавленные растворы, считая, что растворенные вещества распространяются по объему растворителя подобно газу в сосуде, и при помощи закона Авогадро разработал метод определения молекулярной массы растворенных веществ. Закон Авогадро позволил установить истинные атомные массы ряда элементов. Используется при расчетах по химическим формулам и уравнениям химических реакций, для определения относительных молекулярных масс газов, для определения числа молекул в моле любого вещества.
Большой энциклопедический словарь
АВОГАДРО ЗАКОН - в равных объемах идеальных газов при одинаковых давлении и температуре содержится одинаковое число молекул; открыт А. Авогадро в 1811.
Полезные сервисы
авогадро постоянная
Энциклопедический словарь
Авога́дро постоя́нная (число Авогадро; обозначается NA), число молекул или атомов в 1 моле вещества, NA = 6,022045(31)·1023моль-1; названа по имени А. Авогадро.?
* * *
АВОГАДРО ПОСТОЯННАЯ - АВОГА́ДРО ПОСТОЯ́ННАЯ (обозначается NА), число молекул или атомов в 1 моле (см. МОЛЬ) вещества, NА=6,022.1023 моль-1; название в честь А. Авогадро.
Большой энциклопедический словарь
АВОГАДРО ПОСТОЯННАЯ (обозначается NА) - число молекул или атомов в 1 моле вещества, NА=6,022Ч1023 моль-1; название в честь А. Авогадро.
Иллюстрированный энциклопедический словарь
АВОГАДРО ПОСТОЯННАЯ (Авогадро число) (NA), число молекул или атомов в 1 моле вещества; NA=6,022´1023 моль-1. Названа по имени А. Авогадро.
Полезные сервисы
авогадро число
Энциклопедия Кольера
Na = (6,022045±0,000031)*10 23
число молекул в моле любого вещества или число атомов в моле простого вещества. Одна из фундаментальных постоянных, с помощью которой можно определить такие величины, как, например, массу атома или молекулы (см. ниже), заряд электрона и т.д. Моль - количество вещества, которое содержит столько же структурных элементов, сколько атомов содержится в 12 г 12С, причем структурными элементами обычно являются атомы, молекулы, ионы и др. Масса 1 моль вещества, выраженная в граммах, численно равна его мол. массе. Так, 1 моль натрия имеет массу 22,9898 г и содержит 6,02*1023 атомов; 1 моль фторида кальция CaF2 имеет массу (40,08 + 2*18,998) = 78,076 г и содержит 6,02*1023 молекул, как и 1 моль тетрахлорида углерода CCl4, масса которого равна (12,011 + 4*35,453) = 153,823 г и т.п.
Закон Авогадро. На заре развития атомной теории (1811) А. Авогадро выдвинул гипотезу, согласно которой при одинаковых температуре и давлении в равных объемах идеальных газов содержится одинаковое число молекул. Позже было показано, что эта гипотеза есть необходимое следствие кинетической теории, и сейчас она известна как закон Авогадро. Его можно сформулировать так: один моль любого газа при одинаковых температуре и давлении занимает один и тот же объем, при стандартных температуре и давлении (0° С, 1,01*10 5 Па) равный 22,41383 л. Эта величина известна как молярный объем газа. Сам Авогадро не делал оценок числа молекул в заданном объеме, но понимал, что это очень большая величина. Первую попытку найти число молекул, занимающих данный объем, предпринял в 1865 Й.Лошмидт; было установлено, что в 1 см3 идеального газа при нормальных (стандартных) условиях содержится 2,68675Ч1019 молекул. По имени этого ученого указанная величина была названа числом (или постоянной) Лошмидта. С тех пор было разработано большое число независимых методов определения числа Авогадро. Превосходное совпадение полученных значений является убедительным свидетельством реального существования молекул. Метод Лошмидта представляет только исторический интерес. Он основан на предположении, что сжиженный газ состоит из плотноупакованных сферических молекул. Измеряя объем жидкости, которая образовалась из данного объема газа, и зная приблизительно объем молекул газа (этот объем можно было представить исходя из некоторых свойств газа, например вязкости), Лошмидт получил оценку числа Авогадро АВОГАДРО ЧИСЛО10 22. Определение, основанное на измерении заряда электрона. Единица количества электричества, известная как число Фарадея F, - это заряд, переносимый одним молем электронов, т.е. F = Ne, где е - заряд электрона, N - число электронов в 1 моль электронов (т.е. число Авогадро). Число Фарадея можно определить, измеряя количество электричества, необходимое для растворения или осаждения 1 моль серебра. Тщательные измерения, выполненные Национальным бюро стандартов США, дали значение F = 96490,0 Кл, а заряд электрона, измеренный разными методами (в частности, в опытах Р.Милликена), равен 1,602*10-19 Кл. Отсюда можно найти N. Этот метод определения числа Авогадро, по-видимому, является одним из самых точных.
Эксперименты Перрена. Исходя из кинетической теории, было получено включающее число Авогадро выражение, описывающее уменьшение плотности газа (например, воздуха) с высотой столба этого газа. Если бы удалось подсчитать число молекул в 1 см3 газа на двух разных высотах, то, воспользовавшись указанным выражением, мы могли бы найти N. К сожалению, сделать это невозможно, поскольку молекулы невидимы. Однако в 1910 Ж.Перрен показал, что упомянутое выражение справедливо и для суспензий коллоидных частиц, которые видны в микроскопе. Подсчет числа частиц, находящихся на разной высоте в столбе суспензии, дал число Авогадро 6,82Ч1023. Из другой серии экспериментов, в которых измерялось среднеквадратичное смещение коллоидных частиц в результате их броуновского движения, Перрен получил значение N = 6,86Ч1023. В дальнейшем другие исследователи повторили некоторые из экспериментов Перрена и получили значения, хорошо согласующиеся с ныне принятыми. Следует отметить, что эксперименты Перрена стали поворотным моментом в отношении ученых к атомной теории вещества - ранее некоторые ученые рассматривали ее как гипотезу. В.Оствальд, выдающийся химик того времени, так выразил это изменение во взглядах: "Соответствие броуновского движения требованиям кинетической гипотезы... заставило даже наиболее пессимистично настроенных ученых говорить об экспериментальном доказательстве атомной теории".
Расчеты с использованием числа Авогадро. С помощью числа Авогадро были получены точные значения массы атомов и молекул многих веществ: натрия, 3,819*10-23 г (22,9898 г/6,02*10 23), тетрахлорида углерода, 25,54*10-23 г и т.д. Можно также показать, что в 1 г натрия должно содержаться примерно 3*10 22 атомов этого элемента.
См. также АТОМНАЯ МАССА.
ЛИТЕРАТУРА
Основные формулы физики. М., 1957 Гуггенгейм Э., Пру Дж. Физико-химические расчеты. М., 1958
Полезные сервисы
авогадро, амедео
Иллюстрированный энциклопедический словарь
АВОГАДРО (Avogadro) Амедео (1776 - 1856), итальянский физик и химик. Основатель молекулярной теории строения вещества (1811). Установил один из газовых законов (1811; закон Авогадро), согласно которому в равных объемах идеальных газов при одинаковых давлении и температуре содержится одинаковое число молекул.