солеобразова/ние, -я
фенолы
Энциклопедический словарь
Фено́лы - органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН-групп различают фенолы одноатомные (например, фенол), двухатомные (гидрохинон, пирокатехин, резорцин) и т. д. Обладают слабокислотными свойствами, например образуют солеобразные продукты - феноляты. Фенолы выделяют из каменноугольной смолы, синтезируют гидролизом соответствующих галогенопроизводных и другими способами. Применяются в производстве синтетических смол, полиамидов и других полимеров, лекарственных препаратов, красителей, поверхностно-активных веществ, антиоксидантов.
* * *
ФЕНОЛЫ - ФЕНО́ЛЫ, органические соединения ароматического ряда, в молекулах которых гидроксильные группы связаны с атомами углерода ароматического кольца. По числу ОН-групп различают фенолы одноатомные (напр., фенол), двухатомные (гидрохинон, пирокатехин, резорцин) и т. д. Обладают слабокислотными свойствами, напр. образуют солеобразные продукты - феноляты. Фенолы выделяют из каменноугольной смолы, синтезируют гидролизом соответствующих галогенопроизводных и др. способами. Применяются в производстве синтетических смол, полиамидов и др. полимеров, лекарственных препаратов, красителей, поверхностно-активных веществ, антиоксидантов.
Полезные сервисы
стекло неорганическое
Энциклопедический словарь
СТЕКЛО НЕОРГАНИЧЕСКОЕ - СТЕКЛО́ НЕОРГАНИ́ЧЕСКОЕ, квазиаморфное твердое вещество, у которого при наличии ближнего порядка (см. БЛИЖНИЙ ПОРЯДОК) отсутствует дальний порядок (см. ДАЛЬНИЙ ПОРЯДОК И БЛИЖНИЙ ПОРЯДОК) в расположении частиц.
В современном понимании понятие «стекло» определяется не просто как материал, а как некоторое особое стеклообразное состояние твердого тела. Стекло - это такое состояние аморфного вещества, которое получается при затвердевании переохлажденной жидкости. Стекло неравновесно по отношению к кристаллическому состоянию, которое может реализовываться при том же составе и при тех же внешних условиях.
В стеклообразное состояние можно перевести вещества различной природы. Это и расплавы ряда чистых оксидов и их смесей в бесчисленных вариантах, и солеобразные расплавы - галогенидные, нитратные и др. В стеклообразном состоянии легко могут быть получены и многие органические вещества (см. СТЕКЛО ОРГАНИЧЕСКОЕ). Стекла легко образуются водными растворами многих солей и их смесей. В последнее десятилетие стали известны металлические стекла, полученные особо быстрым охлаждением сплавов разных металлов. Таким образом, в стеклообразном состоянии могут находиться вещества самого разного химического типа, с самыми разными видами химических связей - ковалентных, ионных, металлических и разнообразными физико-химическими свойствами.
Впервые человечество познакомилось с природным стеклообразным веществом - обсидианом (см. ОБСИДИАН) - в доисторические времена. Как искусственный материал стекло впервые открыто в Египте ок. 4000 до н. э. На протяжении тысячелетий люди, используя различные добавки, добились большого разнообразия классов и разновидностей стекол. До XIX в. стекло применялось главным образом в изготовлении предметов утилитарного назначения и художественного стекла (см. ХУДОЖЕСТВЕННОЕ СТЕКЛО). В России становление науки о стекле и промышленного стеклоделия связано с именами М. В. Ломоносова (см. ЛОМОНОСОВ Михаил Васильевич) и Д. И. Менделеева (см. МЕНДЕЛЕЕВ Дмитрий Иванович). Ломоносов первым в мировой практике стеклоделия обратил серьезное внимание на взаимосвязь свойств стекол и их химического состава. Заслугой Менделеева являются предвидение полимерного строения SiO2 и развиваемые им представления о химической природе стекла, которое он рассматривал в общем контексте разработки таких фундаментальных понятий химической науки, как определенное-неопределенное соединение, раствор, сплав и т.д.
Структура стекла
Рентгенограммы кварцевого стекла лучше всего интерпретируются в рамках модели непрерывной беспорядочной сетки тетраэдров SiO4 (атом кремния, окружен четырьмя атомами кислорода), и отражают ближний порядок в структуре стекла. Рентгеновские и нейтронографические исследования показали, что наличие неупорядоченной сетки подтверждается применительно к структуре однокомпонентных стекол. В бездефектном кварцевом стекле существуют только мостиковые атомы кислорода. Для стекол, содержащих два или более компонентов, характерна химическая неоднородность. При введении в SiO2 оксида натрия в результате взаимодействия оксидов, несмотря на сохранение координации атомов кремния относительно кислорода, непрерывность кремнекислородной сетки нарушается за счет частичных обрывов связей Si-O-Si, соединяющих тетраэдры между собой.
Состав и свойства стекол
По химическому составу неорганические стекла подразделяют на элементарные, халькогенидные и оксидные. Основу оксидного стекла составляет стеклообразующий оксид. К числу стеклообразующих оксидов относятся SiO2, В2O3, GeO2, P2O5. Наибольшее распространение получили силикатные стекла (на основе SiO2) благодаря высокой химической устойчивости, а также дешевизне и доступности сырьевых компонентов. Для придания определенных физических свойств в состав силикатных стекол вводят оксиды различных металлов (наиболее часто щелочных и щелочноземельных).
Физико-химические свойства стекла зависят от его состава и степени обработки. Наименьшую плотность (СТЕКЛО НЕОРГАНИЧЕСКОЕ2,3 г/см3) имеет кварцевое стекло, состоящее только из оксида кремния. Наиболее тяжелые свинцовые стекла, содержащие много оксида свинца (до 80%), имеют плотность около 8 г/см3.
Предел прочности стекла при растяжении невелик (8.107Н/м2) и увеличивается при повышении содержания в нем SiO2 и CaO. Щелочные оксиды снижают прочность стекла. Сжатию стекло противостоит гораздо лучше, чем растяжению, и предел прочности при сжатии и растяжении может различаться на порядок.
Стекло очень хрупкий материал; наименьшей хрупкостью обладают боросвинцовые стекла. Кварцевое стекло остается хрупким при нагреве до температуры СТЕКЛО НЕОРГАНИЧЕСКОЕ 400°С, при дальнейшем нагреве стекло постепенно размягчается и становится вязкой жидкостью. Процесс перехода стекла из твердого состояния в жидкое не характеризуется сколько-нибудь определенной температурой плавления. При правильном охлаждении жидкого стекла этот процесс происходит в обратном направлении также без кристаллизации (деаморфизации).
Производство
Сырьем для изготовления стекла служат кварцевый песок SiO2, сода Na2CO3, поташ K2CO3, известняк CaCO3, доломит CaCO3.MgCO3, сульфат натрия Na2SO4, бура Na2B4O7, борная кислота H3BO3, сурик Pb3O4, полевой шпат Al2O3.6SiO2.K2O и др. Сырьевые материалы измельчают, отвешивают в нужных соотношениях и тщательно перемешивают. Шихта, как правило, содержит стеклянные осколки, остающиеся от предыдущей варки, и, в зависимости от целей дальнейшего использования стекла, окислители, красители, обесцвечиватели, осветлители, глушители, восстановители и окислители, ускорители варки или иные добавки. Красители придают стеклу нужный цвет. Для этого во время плавки в стеклянную массу добавляют окислы металлов. Например, железо сделает прозрачный материал голубовато-зеленым или желтым, марганец - желтым или коричневым, хром - травянисто-зеленым, уран - желтовато-зеленым (так называемое урановое стекло), кобальт - синим (кобальтовое стекло), коллоидное серебро - желтым, медь - красным. Полученную таким образом шихту загружают в стекловарочную печь. После этого шихту расплавляют при высокой температуре. Стекло варится путем выдерживания смеси сырьевых материалов при температурах от 1200 до 1600°С в течение продолжительного времени - от 12 до 96 ч. При нагреве шихта плавится, летучие составные части (H2O, CO2, SO3) из нее удаляются, а оставшиеся химически реагируют между собой, в результате чего образуется однородная стекломасса, которая идет на выработку листового стекла или стеклянных изделий. Стеклообразное состояние материала получается лишь при быстром охлаждении стекломассы. В случае медленного охлаждения начинается частичная кристаллизация, стекло теряет прозрачность из-за нарушения однородности, а отформованные изделия при этом обладают невысокой механической прочностью.
В процессе охлаждения расплава сильно изменяется вязкость стекломассы. Для любого стекла на графике температурной зависимости вязкости различают две характерные точки, соответствующие температурам текучести Тт и стеклования Тс. При температурах выше Тт у стекла проявляются свойства текучести, типичные для жидкого состояния. Вязкость различных стекол при температуре Тт примерно одинакова и равна 108 Па.с. Температуре стеклования Тс, ниже которой проявляется хрупкость стекла, соответствует вязкость порядка 1012 Па.с. Интервал температур между Тт и Тс называют интервалом размягчения, в котором стекло обладает пластичными свойствами. Для большинства применяемых в технике силикатных стекол Тс=400-600оС, а Тт=700-900оС, т. е. интервал размягчения составляет несколько сотен градусов. Чем шире интервал размягчения, тем технологичнее стекло, так как в этом случае легче отформовать изделия. Изготовленные стеклянные изделия подвергают отжигу с целью устранения возникшего при неравномерном остывании напряжения.
Если в древности варка стекла осуществлялась в глиняных горшочках глубиной и диаметром 5-7 см, то в настоящее время для производства оптического, художественного и других видов стекла специального состава применяют шамотные горшки больших размеров, вмещающие от 200 до 1400 кг шихты. В одной печи могут выдерживаться от 6 до 20 горшков, горшковые печи применяют для получения относительно небольшого количества стекла с точно выдержанным составом. В крупном производстве применяют ванные печи. Большие массы стекла варятся в ванных печах непрерывного действия. Такой режим обеспечивает протекание необходимых химических реакций, в результате чего сырьевая смесь приобретает свойства стекла. Постоянный уровень расплавленного стекла в ванне поддерживается путем непрерывной подачи шихты на одном из концов установки и извлечения готового продукта с той же скоростью из другого конца. В таком режиме некоторые стекловаренные печи работают до пяти лет. Крупные печи, иногда вмещающие несколько сот тонн расплавленного стекла, приспосабливают к интенсивному механическому производству. Как горшковые, так и ванные печи обычно нагревают сжиганием природного газа или мазута.
Силикатное стекло
Силикатные стекла по составу, а в связи с этим и по электрическим, оптическим, механическим свойствам можно разделить на:
- бесщелочные стекла (отсутствуют окислы натрия и калия). В эту группу входит чистое кварцевое стекло. Стекла данной группы обладают высокой устойчивостью к нагреву, высокими электрическими свойствами, но из них трудно изготавливать изделия, особенно сложной конфигурации;
- щелочные стекла без тяжелых окислов или с незначительным их содержанием. Эта группа состоит из двух подгрупп: натриевые и калиевые или калиево-натриевые. В эту группу входит большинство обычных стекол. Они отличаются пониженной устойчивостью к нагреву, легко обрабатываются при нагреве, но имеют пониженные электрические свойства: снижается удельное сопротивление, возрастают диэлектрические потери;
- щелочные стекла с высоким содержанием тяжелых оксидов (например, силикатно-свинцовые или бариевые).
Электропроводящие прозрачные покрытия
Был открыт целый ряд необычных применений стекла в связи с тем, что ему можно придать свойство поверхностной проводимости. Это достигается напылением на поверхность стеклянного изделия тонкого, прозрачного, почти невидимого слоя оксида металла. Электропроводящая пленка (толщиной 0,5 мкм), например, может быть получена напылением солей металлического серебра и нагревом стекла до температуры 500-700 °С. Такое покрытие весьма долговечно и имеет поверхностное сопротивление в пределах от 10 до 100 Ом/см2. После покрытия пленки тонким слоем люминофора стекло можно использовать в качестве светящегося элемента (с голубым, зеленым, желтым свечением). При обычных температурах можно использовать известковое стекло, а при высоких - боросиликатное. Изготовленные из такого стекла панели лучистого нагрева могут работать при температурах до 350° С. Подобные панели - хороший источник энергии длинноволнового инфракрасного излучения, которое большинство веществ и сред поглощает с эффективностью 90% и более. Таким способом изготавливаются настольные стеклянные излучатели и вспомогательные нагреватели для помещений. Проводящие покрытия, нанесенные на ветровые стекла самолетов, сохраняют их теплыми и свободными от льда. Кроме того, в качестве источника тепла используют стеклопакеты с внутренним слоем из электропроводящего стекла.
Электротехнические изделия
Стеклянные колбы широко используются в качестве оболочек для ламп накаливания и электронно-лучевых трубок. Проволочные резисторы, трансформаторы, конденсаторы, реле и переключатели могут заключаться в оболочки из отпущенного стекла с выводами через стеклянные изоляторы. Крупные проходные изоляторы массой до 22 кг, рассчитанные на сильные токи и высокие напряжения, изготавливаются путем центробежной отливки стекла вокруг металлических втулок. С применением стекла изготавливаются конденсаторы как постоянной, так и переменной емкости. В конденсаторах постоянной емкости используется листовое стекло толщиной до 0,025 мм. Конденсатор переменной емкости состоит из изготовленной с жестким допуском стеклянной трубки, часть внешней поверхности которой металлизируется для образования одной обкладки. Внутрь трубки вставляется стержень из латуни или инвара, образующий вторую обкладку. Стеклянные трубки или стержни с нанесенной на них углеродной, металлической или металлооксидной пленкой используются в качестве резисторов (см. РЕЗИСТОР).
Устойчивость к радиоактивности
Стекло, устойчивое к радиоактивному излучению, получают из шихты специального состава. Для поглощения рентгеновских лучей используют оптические стекла с высоким содержанием свинца и бора. Чтобы улучшить устойчивость стекла к излучению, в шихту добавляют 0,25-1,5% окиси церия. Защитные свойства стекла можно приближенно оценивать по их плотности. Например, тяжелое свинцовое стекло с объемной массой 6200 кг/м3, содержащее 80% окиси свинца, по своей защитной способности в отношении излучения эквивалентно стали. Стекла, поглощающие медленные нейтроны, должны содержать один из следующих окислов: окись бора, окись лития, окись кадмия и др. Стекло, устойчивое к действию радиоактивных излучений, применяют при сооружении атомных электростанций (например, при устройстве защитных смотровых окон) и предприятий по изготовлению изотопов.
Светочувствительные стекла
В 1947 было обнаружено, что стекла некоторых составов при воздействии ультрафиолетового излучения образуют скрытое изображение, которое может быть проявлено путем нагрева стекла чуть выше температуры отжига. Например, на стекло можно наложить фотографический негатив и облучить его ультрафиолетом, а потом нагреть стекло; в результате в объеме стекла появится воспроизведенное в цвете изображение. Цвет изображения зависит от вида светочувствительного металла, введенного в шихту. Один из составов дает опаловое стекло такой природы, что разбавленная фтористоводородная кислота протравливает облученную часть раз в пятнадцать быстрее, чем необлученную. Эта огромная разница в растворимостях позволяет осуществлять химическое травление. Таким способом в стекле можно вытравливать отверстия размером меньше половины среднего диаметра человеческого волоса в количестве до 100 тыс. отверстий на 1 см2. Стекла этого типа используются для изготовления световых табло и элементов светового декора, а также в качестве чувствительных элементов дозиметров. После воздействия проникающего излучения некоторые из таких стекол ярко светятся при облучении ультрафиолетовым светом, а другие меняют свой цвет. Интенсивность флуоресценции (см. ФЛУОРЕСЦЕНЦИЯ) или степень изменения окраски пропорциональна полученной дозе облучения.
Пористые стекла
Варьирование химического состава стекол, режимов отжига и последующей обработки разными растворителями позволило получать стекла с размером пор от нескольких десятков до 1000 ангстрем. Пористые стекла широко применяются как адсорбенты и как «молекулярные сита», которые пропускают мелкие молекулы и не пропускают более крупные. Молекулярные сита были использованы, например, при получении противогриппозных вакцин. При введении в поры каких-либо неорганических соединений и последующей термообработке при 1000 - 1200оС получаются разнообразнейшие материалы, называемые импрегнированными кварцоидами. Они представляют собой массивное, во многих случаях совершенно прозрачное стекло, в котором уже нет пор. Это стекло обладает особыми свойствами, определяемыми составом введенных в поры веществ.
Оптические стекла
Значительную долю в производстве оптического стекла составляет оптическое стекло со специальными свойствами:
- лазерное стекло на силикатной и фосфатной основе с различными концентрациями активатора, позволяющее создавать твердотельные квантовые генераторы, которые используются в научных исследованиях, медицине, специальных дальномерах и прицелах;
- бескислородные или халькогенидные стекла для инфракрасной области спектра, применяются в оптических и полупроводниковых системах. Созданы особо чистые высокооднородные стекла, которые применяются в рентгеновских установках для защиты от излучения, используются в создании оптических систем для микролитографии, и позволяют получить микросхемы с разрешающей способностью менее микрона и обеспечить цветопередачу ТВ-систем;
- на основе стекловолокна изготавливают волоконно-оптические элементы для передачи света и изображения. Применяются в космических аппаратах, военной технике, цветном телевидении, медицине, приборах ночного видения.
Фотохромные стекла
Фотохромными называются стекла, изменяющие окраску под действием излучения. В настоящее время получили распространение очки со стеклами-«хамелеонами», которые при освещении темнеют, а в отсутствие интенсивного освещения вновь становятся бесцветными. Такие стекла применяют для защиты от солнца сильно остекленных зданий и для поддержания постоянной освещенности помещений, а также на транспорте. Фотохромные стекла содержат оксид бора B2O3, а светочувствительным компонентом является хлорид серебра AgCl в присутствии оксида меди Cu2O. При освещении в результате химической реакции выделяется атомарное серебро, что приводит к потемнению стекла. В темноте реакция протекает в обратном направлении. Оксид меди играет роль своеобразного катализатора. При интенсивном облучении стекла (в том числе и лабораторного) г-лучами нейтронами и в меньшей мере б-, и в-лучами также происходит окрашивание стекла (чаще в темные и черные цвета). Это связано с изменением структуры стекла и образованием ионов, которые играют роль «цветовых центров». При нагревании стекла до температур, близких к температуре размягчения, окраска исчезает. Иногда подобные стекла используют в качестве дозиметров больших доз излучений.
Халькогенидные стекла
Считаются весьма интересной и перспективной в практическом отношении группой веществ, сочетающих в себе свойства стекол и кристаллических тел полупроводников. Известны они очень давно. Например, одно из первых упоминаний о такого рода стеклах относится еще к 19 в. (стекло состава As2S3). Однако как определенный класс стекол они стали изучаться лишь в 1970-х гг., когда было установлено, что сплавы халькогенидов - сурьмы, мышьяка и таллия - образуют обширную область стеклообразного состояния. Халькогенидные стекла могут быть получены на основе самых различных сочетаний. В совокупности они представляют весьма обширную группу стекол, обладающих весьма разнообразными физико-химическими, физическими, электрическими и оптическими свойствами. Электропроводность халькогенидных стекол в зависимости от состава может находиться в границах 10-14-10-1ом-1·см-1, т. е. быть выше электропроводности многих известных кристаллических проводников. Изучение электрических свойств этой группы веществ показало, что по ряду признаков (температурная проводимость, большое значение термоэлектродвижущей силы, и особенно внутренний фотоэлектрический эффект) они являются типичными электронными полупроводниками с дырочным механизмом проводимости. Соединения такого типа в последние годы стали применять в переключающих устройствах, нелинейной оптике и в качестве стеклообразующих полупроводников.
На основе стекол также получают: стеклокерамический материал - ситалл (см. СИТАЛЛЫ), ячеистый материал пеностекло (см. ПЕНОСТЕКЛО), триплекс (см. ТРИПЛЕКС), и ряд других материалов.
Полезные сервисы
азот
Энциклопедический словарь
АЗО́Т -а; м. [франц. azote от греч. an- не-, без- и zōtikos - дающий жизнь]. Химический элемент (N), газ без цвета и запаха, не поддерживающий дыхания и горения (составляет основную по объёму и массе часть воздуха, является одним из главных элементов питания растений).
◁ Азо́тный, -ая, -ое. А-ая кислота. А-ые удобрения. Азо́тистый, -ая, -ое. А-ая кислота.
* * *
азо́т (лат. Nitrogenium), химический элемент V группы периодической системы. Название от греч. а... - отрицательная приставка, и zōē - жизнь (не поддерживает дыхания и горения). Свободный азот состоит из 2-атомных молекул (N2); газ без цвета и запаха; плотность 1,25 г/л, tпл -210ºC, tкип -195,8ºC. Химически весьма инертен, однако реагирует с комплексными соединениями переходных металлов. Основной компонент воздуха (78,09% объёма), разделением которого получают промышленный азот (более 3/4 идёт на синтез аммиака). Применяется как инертная среда для многих технологических процессов; жидкий азот - хладагент. Азот - один из основных биогенных элементов, входящий в состав белков и нуклеиновых кислот.
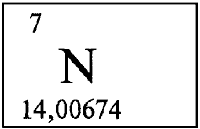
* * *
АЗОТ - АЗО́Т (лат. Nitrogenium - рождающий селитры), N (читается «эн»), химический элемент второго периода VA группы периодической системы, атомный номер 7, атомная масса 14,0067. В свободном виде - газ без цвета, запаха и вкуса, плохо растворим в воде. Состоит из двухатомных молекул N2, обладающих высокой прочностью. Относится к неметаллам.
Природный азот состоит из стабильных нуклидов (см. НУКЛИД) 14N (содержание в смеси 99,635% по массе) и 15N. Конфигурация внешнего электронного слоя 2s22р3. Радиус нейтрального атома азота 0,074 нм, радиус ионов: N3- - 0,132 , N3+ - 0,030 и N5+ - 0,027 нм. Энергии последовательной ионизации нейтрального атома азота равны, соответственно, 14,53, 29,60, 47,45, 77,47 и 97,89 эВ. По шкале Полинга электроотрицательность азота 3,05.
История открытия
Открыт в 1772 шотландским ученым Д. Резерфордом в составе продуктов сжигания угля, серы и фосфора как газ, непригодный для дыхания и горения («удушливый воздух») и в отличие от CO2 не поглощаемый раствором щелочи. Вскоре французский химик А. Л. Лавуазье (см. ЛАВУАЗЬЕ Антуан Лоран) пришел к выводу, что «удушливый» газ входит в состав атмосферного воздуха, и предложил для него название «azote» (от греч. azoos - безжизненный). В 1784 английский физик и химик Г. Кавендиш (см. КАВЕНДИШ Генри) установил присутствие азота в селитре (отсюда латинское название азота, предложенное в 1790 французским химиком Ж. Шанталем).
Нахождение в природе
В природе свободный (молекулярный) азот входит в состав атмосферного воздуха (в воздухе 78,09% по объему и 75,6% по массе азота), а в связанном виде - в состав двух селитр: натриевой NaNO3 (встречается в Чили, отсюда название чилийская селитра (см. ЧИЛИЙСКАЯ СЕЛИТРА)) и калиевой KNO3 (встречается в Индии, отсюда название индийская селитра) - и ряда других соединений. По распространенности в земной коре азот занимает 17-е место, на его долю приходится 0,0019% земной коры по массе. Несмотря на свое название, азот присутствует во всех живых организмах (1-3% на сухую массу), являясь важнейшим биогенным элементом (см. БИОГЕННЫЕ ЭЛЕМЕНТЫ). Он входит в состав молекул белков, нуклеиновых кислот, коферментов, гемоглобина, хлорофилла и многих других биологически активных веществ. Некоторые, так называемые азотфиксирующие, микроорганизмы способны усваивать молекулярный азот воздуха, переводя его в соединения, доступные для использования другими организмами (см. Азотфиксация (см. АЗОТФИКСАЦИЯ)). Превращения соединений азота в живых клетках - важнейшая часть обмена веществ у всех организмов.
Получение
В промышленности азот получают из воздуха. Для этого воздух сначала охлаждают, сжижают, а жидкий воздух подвергают перегонке (дистилляции). Температура кипения азота немного ниже (-195,8 °C), чем другого компонента воздуха - кислорода (-182,9 °C), поэтому при осторожном нагревании жидкого воздуха азот испаряется первым. Потребителям газообразный азот поставляют в сжатом виде (150 атм. или 15 МПа) в черных баллонах, имеющих желтую надпись «азот». Хранят жидкий азот в сосудах Дьюара (см. ДЬЮАРА СОСУД).
В лаборатории чистый («химический») азот получают, добавляя при нагревании насыщенный раствор хлорида аммония NH4Cl к твердому нитриту натрия NaNO2:
NaNO2 + NH4Cl = NaCl + N2 + 2H2O.
Можно также нагревать твердый нитрит аммония:
NH4NO2 = N2 + 2H2O.
Физические и химические свойства
Плотность газообразного азота при 0 °C 1,25046 г/дм3, жидкого азота (при температуре кипения) - 0,808 кг/дм3. Газообразный азот при нормальном давлении при температуре -195,8 °C переходит в бесцветную жидкость, а при температуре -210,0 °C - в белое твердое вещество. В твердом состоянии существует в виде двух полиморфных модификаций: ниже -237,54 °C устойчива форма с кубической решеткой, выше - с гексагональной.
Критическая температура азота -146,95 °C, критическое давление 3,9МПа, тройная точка лежит при температуре -210,0 °C и давлении 125,03 гПа, из чего следует, что азот при комнатной температуре ни при каком, даже очень высоком давлении, нельзя превратить в жидкость.
Теплота испарения жидкого азота 199,3 кДж/кг (при температуре кипения), теплота плавления азота 25,5 кДж/кг (при температуре -210 °C).
Энергия связи атомов в молекуле N2 очень велика и составляет 941,6 кДж/моль. Расстояние между центрами атомов в молекуле 0,110 нм. Это свидетельствует о том, что связь между атомами азота тройная. Высокая прочность молекулы N2 может быть объяснена в рамках метода молекулярных орбиталей. Энергетическая схема заполнения молекулярных орбиталей в молекуле N2 показывает, что электронами в ней заполнены только связывающие s- и p-орбитали. Молекула азота немагнитна (диамагнитна).
Из-за высокой прочности молекулы N2процессы разложения различных соединений азота (в том числе и печально знаменитого взрывчатого вещества гексогена (см. ГЕКСОГЕН)) при нагревании, ударах и т. д. приводят к образованию молекул N2. Так как объем образовавшегося газа значительно больше, чем объем исходного взрывчатого вещества, гремит взрыв.
Химически азот довольно инертен и при комнатной температуре реагирует только с металлом литием (см. ЛИТИЙ) с образованием твердого нитрида лития Li3N. В соединениях проявляет различные степени окисления (от -3 до +5). С водородом образует аммиак (см. АММИАК) NH3. Косвенным путем (не из простых веществ) получают гидразин (см. ГИДРАЗИН) N2H4 и азотистоводородную кислоту HN3. Соли этой кислоты - азиды (см. АЗИДЫ). Азид свинца Pb(N3)2 разлагается при ударе, поэтому его используют как детонатор, например, в капсюлях патронов.
Известно несколько оксидов азота (см. АЗОТА ОКСИДЫ). С галогенами азот непосредственно не реагирует, косвенными путями получены NF3, NCl3, NBr3 и NI3, а также несколько оксигалогенидов (соединений, в состав которых, кроме азота, входят атомы и галогена, и кислорода, например, NOF3).
Галогениды азота неустойчивы и легко разлагаются при нагревании (некоторые - при хранении) на простые вещества. Так, NI3 выпадает в осадок при сливании водных растворов аммиака и иодной настойки. Уже при легком сотрясении сухой NI3 взрывается:
2NI3 = N2 + 3I2.
Азот не реагирует с серой, углеродом, фосфором, кремнием и некоторыми другими неметаллами.
При нагревании азот реагирует с магнием и щелочноземельными металлами, при этом возникают солеобразные нитриды общей формулы М3N2, которые разлагаются водой с образованием соответствующих гидроксидов и аммиака, например:
Са3N2 + 6H2O = 3Ca(OH)2 + 2NH3.
Аналогично ведут себя и нитриды щелочных металлов. Взаимодействие азота с переходными металлами приводит к образованию твердых металлоподобных нитридов различного состава. Например, при взаимодействии железа и азота образуются нитриды железа состава Fe2N и Fe4N. При нагревании азота с ацетиленом C2H2 может быть получен цианистый водород HCN.
Из сложных неорганических соединений азота наибольшее значение имеют азотная кислота (см. АЗОТНАЯ КИСЛОТА) HNO3, ее соли нитраты (см. НИТРАТЫ), а также азотистая кислота HNO2 и ее соли нитриты (см. НИТРИТЫ).
Применение
В промышленности газ азот используют главным образом для получения аммиака (см. АММИАК). Как химически инертный газ азот применяют для обеспечения инертной среды в различных химических и металлургических процессах, при перекачке горючих жидкостей. Жидкий азот широко используют как хладагент (см. ХЛАДАГЕНТ), его применяют в медицине, особенно в косметологии. Важное значение в поддержании плодородия почв имеют азотные минеральные удобрения (см. МИНЕРАЛЬНЫЕ УДОБРЕНИЯ).