МАРГАНЕЦ (химический элемент) - МА́РГАНЕЦ (лат. Manganum), Mn, химический элемент с атомным номером 25, атомная масса 54,9380. Химический символ элемента Mn произносится так же, как и название самого элемента. Природный марганец состоит только из нуклида (см. НУКЛИД) 55Mn. Конфигурация двух внешних электронных слоев атома марганца 3s2p6d54s2. В периодической системе Д. И. Менделеева марганец входит в группу VIIВ, к которой относятся также технеций (см. ТЕХНЕЦИЙ) и рений (см. РЕНИЙ), и располагается в 4-м периоде. Образует соединения в степенях окисления от +2 (валентность II) до +7 (валентность VII), наиболее устойчивы соединения, в которых марганец проявляет степени окисления +2 и +7. У марганца, как и у многих других переходных металлов, известны также соединения, содержащие атомы марганца в степени окисления 0.
Радиус нейтрального атома марганца 0,130 нм, радиус иона Mn2+ - 0,080-0,104 нм, иона Mn7+ - 0,039-0,060 нм. Энергии последовательной ионизации атома марганца 7,435, 15,64, 33,7, 51,2, 72,4 эВ. По шкале Полинга электроотрицательность марганца 1,55; марганец принадлежит к числу переходных металлов. Марганец в компактном виде - твердый серебристо-белый металл.
История открытия
Один из основных материалов марганца - пиролюзит (см. ПИРОЛЮЗИТ)- был известен в древности как черная магнезия и использовался при варке стекла для его осветления. Его считали разновидностью магнитного железняка, а тот факт, что он не притягивается магнитом, Плиний Старший объяснил женским полом черной магнезии, к которому магнит «равнодушен». В 1774 г. шведский химик К. Шееле (см. ШЕЕЛЕ Карл Вильгельм) показал, что в руде содержится неизвестный металл. Он послал образцы руды своему другу химику Ю. Гану (см. ГАН Юхан Готлиб) , который, нагревая в печке пиролюзит с углем, получил металлический марганец. В начале 19 в. для него было принято название «манганум» (от немецкого Manganerz - марганцевая руда).
Нахождение в природе
В земной коре содержание марганца составляет около 0,1 % по массе. В свободном виде марганец не встречается. Из руд наиболее распространены пиролюзит MnO2(содержит 63,2 % марганца), манганит (см. МАНГАНИТ) MnO2·Mn(OH)2 (62,5 % марганца), браунит (см. БРАУНИТ) Mn2O3 (69,5 % марганца), родохрозит (см. РОДОХРОЗИТ) MnCo3 (47,8 % марганца), псиломелан (см. ПСИЛОМЕЛАН) mMnO·MnO2·nH2O (45-60% марганца). Марганец содержат жՐېՐאޭмарганцевые конкреции, которые в больших количествах (сотни миллиардов тонн) находятся на дне Тихого, Атлантического и Индийского океанов. В морской воде содержится около 1,0·10-8 % марганца. Промышленного значения эти запасы марганца пока не имеют из-за сложности подъема конкреций на поверхность.
Получение
Промышленное получение марганца начинается с добычи и обогащения руд. Если используют карбонатную руду марганца, то ее предварительно подвергают обжигу. В некоторых случаях руду далее подвергают сернокислотному выщелачиванию. Затем обычно марганец в полученном концентрате восстанавливают с помощью кокса (карботермическое восстановление). Иногда в качестве восстановителя используют алюминий или кремний. Для практических целей чаще всего используют ферромарганец, полученный в доменном процессе (см. ст. Железо (см. ЖЕЛЕЗО)) при восстановлении руд железа и марганца коксом (см. КОКС). В ферромарганце содержание углерода составляет 6-8 % по массе. Чистый марганец получают электролизом водных растворов сульфата марганца MnSO4, который проводят в присутствии сульфата аммония (NH4)2SO4.
Физические и химические свойства
Марганец твердый хрупкий металл. Известны четыре кубические модификации металлического марганца. При температурах от комнатной и до 710°C устойчив альфа-Mn, параметр решетки а = 0,89125 нм, плотность 7,44 кг/дм3. В интервале температур 710-1090°C существует бета-Mn, параметр решетки а = 0,6300 нм; при температурах 1090-1137°C - гамма-Mn, параметр решетки а = 0,38550 нм. Наконец, при температуре от 1137°C и до температуры плавления (1244°C) устойчив дельта-Mn с параметром решетки а = 0,30750 нм. Модификаци альфа, бета и дельта хрупкие, гамма-Mn пластичен. Температура кипения марганца около 2080°C.
На воздухе марганец окисляется, в результате чего его поверхность покрывается плотной оксидной пленкой, которая предохраняет металл от дальнейшего окисления. При прокаливании на воздухе выше 800°C марганец покрывается окалиной, состоящей из внешнего слоя Mn3O4 и внутреннего слоя состава MnO. Марганец образует несколько оксидов: MnO, Mn3O4, Mn2O3, MnO2 и Mn2O7. Все они, кроме Mn2O7, представляющего собой при комнатной температуре маслянистую зеленую жидкость с температурой плавления 5,9°C, твердые кристаллические вещества. Монооксид марганца MnO образуется при разложении солей двухвалентного марганца (карбоната и других) при температуре около 300°C в инертной атмосфере:
MnCO3 = MnO + CO2
Этот оксид обладает полупроводниковыми свойствами. При разложении MnOОН можно получить Mn2O3. Этот же оксид марганца образуется при нагревании MnO2 на воздухе при температуре примерно 600°C:
4MnO2 = 2Mn2O3 + O2
Оксид Mn2O3 восстанавливается водородом до MnO, а под действием разбавленных серной и азотной кислот переходит в диоксид марганца MnO2. Если MnO2 прокаливать при температуре около 950°C, то наблюдается отщепление кислорода и образование оксида марганца состава Mn3O4:
3MnO2 = Mn3O4 + O2
Этот оксид можно представить как MnO·Mn2О3, и по свойствам Mn3О4 соответствует смеси этих оксидов. Диоксид марганца MnO2 - наиболее распространенное природное соединение марганца в природе, существующее в нескольких полиморфных формах. Так называемая бета-модификация MnO2 - это уже упоминавшийся минерал пиролюзит. Ромбическая модификация диоксида марганца, гамма-MnO2 также встречается в природе. Это - минерал рамсделит (другое название - полианит).
Диоксид марганца нестехиометричен, в его решетке всегда наблюдается дефицит кислорода. Если оксиды марганца, отвечающие его более низким степеням окисления, чем +4, - основные, то диоксид марганца обладает амфотерными свойствами. При 170°C MnO2 можно восстановить водородом до MnO. Если к перманганату калия KMnO4 добавить концентрированную серную кислоту, то образуется кислотный оксид Mn2O7, обладающий сильными окислительными свойствами:
2KMnO4 + 2H2SO4 = 2KHSO4 + Mn2O7 + H2O.
Mn2O7 - кислотный оксид, ему отвечает сильная, не существующая в свободном состоянии марганцовая кислота НMnO4. При взаимодействии марганца с галогенами образуются дигалогениды MnHal2. В случае фтора возможно также образование фторидов состава MnF3 и MnF4, а в случае хлора - также трихлорида MnCl3. Реакции марганца с серой приводят к образованию сульфидов составов MnS (существует в трех полиморфных формах) и MnS2. Известна целая группа нитридов марганца: MnN6, Mn5N2, Mn4N, MnN, Mn6N5, Mn3N2.
С фосфором марганец образует фосфиды составов MnР, MnP3, Mn2P, Mn3P, Mn3P2 и Mn4P. Известно несколько карбидов и силицидов марганца. С холодной водой марганец реагирует очень медленно, но при нагревании скорость реакции значительно возрастает, образуется Mn(OH)2 и выделяется водород. При взаимодействии марганца с кислотами образуются соли марганца(II):
Mn + 2HCl = MnCl2 + H2.
Из растворов солей Mn2+ можно осадить плохо растворимое в воде основание средней силы Mn(OH)2:
Mn(NO3)2 + 2NaOH = Mn(OH)2 + 2NaNO3
Марганцу отвечает несколько кислот, из которых наиболее важны сильные неустойчивые марганцоватая кислота H2MnO4 и марганцовая кислота HMnO4, соли которых - соответственно, манганаты (например, манганат натрия Na2MnO4) и перманганаты (например, перманганат калия KMnO4). Манганаты (известны манганаты только щелочных металлов и бария) могут проявлять свойства как окислителей (чаще)
2NaI + Na2MnO4 + 2H2O = MnO2 + I2 + 4NaOH,
так и восстановителей
2K2MnO4 + Cl2 = 2KMnO4 + 2KCl.
В водных растворах манганаты диспропорционируют на соединения марганца(+4) и марганца(+7):
3K2MnO4 + 3Н2О = 2KMnO4 + MnO2·Н2О + 4КОН.
При этом окраска раствора из зеленой переходит в синюю, затем в фиолетовую и малиновую. За способность изменять окраску своих растворов К. Шееле назвал манганат калия минеральным хамелеоном. Перманганаты - сильные окислители. Например, перманганат калия KMnO4 в кислой среде окисляет сернистый газ SO2 до сульфата:
2KMnO4 + 5SO2 +2H2O = K2SO4 + 2MnSO4 + 2H2SO4. При давлении около 10 МПа безводный MnCl2 в присутствии металлоорганических соединений реагирует с оксидом углерода(II) CO с образованием биядерного карбонила Mn2(CO)10.
Применение
Более 90% производимого марганца идет в черную металлургию. Марганец используют как добавку к сталям для их раскисления (см. РАСКИСЛЕНИЕ), десульфурации (см. ДЕСУЛЬФУРАЦИЯ) (при этом происходит удаление из стали нежелательных примесей - кислорода, серы), а также для легирования (см. ЛЕГИРОВАНИЕ) сталей, т. е. улучшения их механических и коррозионных свойств. Марганец применяется также в медных, алюминиевых и магниевых сплавах. Покрытия из марганца на металлических поверхностях обеспечивают их антикоррозионную защиту. Для нанесения тонких покрытий из марганца используют легко летучий и термически нестабильный биядерный декакарбонил Mn2(CO)10. Соединения марганца (карбонат, оксиды и другие) используют при производстве ферритных материалов, они служат катализаторами (см. КАТАЛИЗАТОРЫ) многих химических реакций, входят в состав микроудобрений.
Биологическая роль
Марганец - микроэлемент (см. МИКРОЭЛЕМЕНТЫ), постоянно присутствующий в живых организмах и необходимый для их нормальной жизнедеятельности. Содержание марганца в растениях составляет 10-4-10-2 %, в животных 10-3-10-5%, некоторые растения (водяной орех, ряска, диатомовые водоросли) и животные (муравьи, устрицы, ряд ракообразных) способны концентрировать марганец. В организме среднего человека (масса тела 70 кг) содержится 12 мг марганца. Марганец необходим животным и растениям для нормального роста и размножения. Он активирует ряд ферментов, участвует в процессах дыхания, фотосинтеза (см. ФОТОСИНТЕЗ), влияет на проветривание и минеральные обмен.
Человек с пищей получает ежедневно 0,4-10 мг марганца. Недостаток марганца в организме может привести к заболеванию человека. Для обеспечения нормального развития растений в почву вносят марганцевые микроудобрения (обычно в форме разбавленного раствора перманганата калия). Однако избыток марганца для человеческого организма вреден. При отравлении соединениями марганца происходит поражение нервной системы, развивается так называемый марганцевый паркинсонизм. (см. ПАРКИНСОНИЗМ)ПДК в расчете на марганец для воздуха 0,03 мг/м3. Токсическая доза (для крыс) - 10-20 мг.
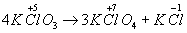 . Диспропорционирование в органической химии - обычно перераспределение атомов или их группировок между двумя одинаковыми молекулами, например,
. Диспропорционирование в органической химии - обычно перераспределение атомов или их группировок между двумя одинаковыми молекулами, например,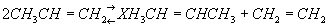 .
.